رادیولیز چیست؟ مرجع کامل تجزیه پرتویی در علم پلیمر

زمانی که یک قطعه پلیمری در معرض تابشهای پرانرژی قرار میگیرد، دقیقاً چه اتفاقی در سطح مولکولی رخ میدهد؟ آیا انرژی جذب شده صرفاً باعث گرم شدن ماده میشود یا تغییراتی اساسی و ساختاری را ایجاد میکند؟ بسیاری از مهندسین با این چالش مواجه شدهاند که چرا برخی پلاستیکها پس از تابشدهی خواص مکانیکی بهتری پیدا میکنند، در حالی که برخی دیگر به سرعت تخریب شده و به پودری شکننده تبدیل میشوند. درک دقیق اینکه چگونه یک پرتو نامرئی میتواند ساختار فیزیکی و شیمیایی یک ماکرومولکول را تغییر دهد، چالش اصلی در طراحی مواد مقاوم و کارآمد است.
ما در این مقاله به توضیح علمی پدیده رادیولیز میپردازیم و مکانیزمهای آن را در ساختارهای مختلف پلیمری تحلیل میکنیم. هدف این است که با شناخت دقیق فرآیندهای تجزیه پرتویی، دیدگاهی فنی و شفاف برای صنعتگران و پژوهشگران فراهم شود تا بتوانند رفتار مواد را در برابر منابع تابشی پیشبینی و مدیریت کنند. بررسی عمیق این واکنشها به شناخت مرز باریک میان تخریب ناخواسته و اصلاح خواص مطلوب در مهندسی پلیمر کمک میکند.
- رادیولیز چیست؟
- تفاوت رادیولیز با سایر روشهای تخریب
- مراحل زمانی رادیولیز
- انتقال انرژی خطی (LET) در رادیولیز
- نظریه ردپا (Spur Theory) در توزیع انرژی
- نقش الکترونهای ثانویه در فرآیند رادیولیز
- مکانیزم تشکیل رادیکالهای آزاد پلیمری
- انواع رادیکالهای ماکرومولکولی
- واکنشهای انتقال هیدروژن در زنجیره پلیمر
- مکانیزم دقیق قطع زنجیر (Chain Scission)
- مکانیزم دقیق شبکهای شدن (Cross-linking)
- اثر قفس (Cage Effect) در بازترکیب رادیکالها
- تشکیل پیوندهای غیراشباع و تغییر رنگ پلیمر
- تولید گازهای رادیولیتیک در پلیمرها ($H_2$, $CO$, $CO_2$, $CH_4$)
- روشهای آنالیز تغییرات ناشی از رادیولیز
- کاربرد رزونانس اسپین الکترون (ESR) در شناسایی رادیکالها
- آنالیز طیفسنجی مادون قرمز (FTIR) برای تغییرات ساختاری
- استفاده از کروماتوگرافی گازی (GC) برای تحلیل گازهای خروجی
- اندازهگیری تغییرات وزن مولکولی با ویسکومتری
- بررسی تغییرات خواص حرارتی با DSC و TGA
- آنالیز تغییرات سطح پلیمر با میکروسکوپ الکترونی (SEM)
- تاثیر متغیرهای محیطی بر رادیولیز
- رفتار رادیولیز در پلیاولفینها (PE, PP)
- حساسیت پرتویی در پلیمرهای هالوژندار (PVC, PTFE)
- پایداری پرتویی در پلیمرهای آروماتیک (PS, PET)
- رادیولیز در پلیمرهای زیستتخریبپذیر (PLA, Starch)
- اثر پرتو بر سلولز و پلیمرهای طبیعی
- تخریب پرتویی در پلیآمیدها و نایلونها
- رفتار رزینهای اپوکسی و گرماسختها در برابر پرتو
- رادیولیز در لاستیکهای سیلیکونی (PDMS)
- کاربردهای نوین رادیولیز در صنعت
- روشهای پایدارسازی پلیمر در برابر پرتو
- افزودنیهای محافظ پرتویی (Antirads)
رادیولیز چیست؟
رادیولیز (Radiolysis) یا همان تجزیه پرتویی، به مجموعهای از تغییرات شیمیایی و فیزیکی گفته میشود که منشأ اصلی آنها جذب انرژی از تابشهای یونساز است. در علم مواد و بهویژه مهندسی پلیمر، ما این پدیده را به عنوان برهمکنش مستقیم پرتوهای پرانرژی با ابر الکترونی اتمهای تشکیلدهنده زنجیره پلیمری میشناسیم. برخلاف واکنشهای شیمیایی متداول که معمولاً با کاتالیزور یا گرما آغاز میشوند، در این فرآیند، انرژی تابشی به تنهایی و با شدت بالا وضعیت پایداری ماده را بر هم میزند.

نکته کلیدی برای درک صحیح ماهیت رادیولیز، توجه به تفاوت سطح انرژیها است. انرژی پیوندهای کووالانسی (مانند پیوند C-C یا C-H) که اسکلت اصلی یک پلیمر را تشکیل میدهند، معمولاً در محدودهای پایین و در حدود چند الکترونولت (eV) قرار دارد. این در حالی است که پرتوهای وارد شده به سیستم، حامل انرژیهایی بسیار بالاتر (در مقیاس کیلو یا مگا الکترونولت) هستند. زمانی که این حجم عظیم انرژی به ساختار مولکولی برخورد میکند، پلیمر نمیتواند آن را به صورت ارتعاشات حرارتی دفع کند و ناچاراً دچار تغییرات آنی در ساختار الکترونی خود میشود.
ما در بررسی این پدیده مشاهده میکنیم که تجزیه پرتویی خاصیتی غیرگزینشپذیر دارد. به این معنی که پرتو در حین عبور از ماتریس پلیمر، به صورت تصادفی با الکترونهای لایههای مختلف اتمها برخورد میکند و انرژی خود را به آنها منتقل میسازد. این انتقال انرژی منجر به ایجاد حفرههای یونی، الکترونهای آزاد و مولکولهای برانگیخته میشود. در واقع، رادیولیز مرحلهای است که در آن یک ماده خنثی و پایدار، تحت شوک انرژی خارجی به مجموعهای از گونههای ناپایدار و واکنشپذیر تبدیل میشود که پتانسیل تغییرات ساختاری عمیق را در خود دارند.
تفاوت رادیولیز با سایر روشهای تخریب
تشخیص مرز میان رادیولیز و سایر مکانیزمهای تخریب پلیمر، برای درک صحیح رفتار ماده ضروری است. اگرچه نتیجه نهایی در بسیاری از موارد مشابه به نظر میرسد، مانند کاهش خواص مکانیکی یا تغییر رنگ اما مسیری که مولکولها طی میکنند تا به این نقطه برسند، کاملاً متفاوت است. ما عمدهترین تفاوت را در “مقدار انرژی” و “نحوه توزیع” آن در ساختار ماده جستجو میکنیم.

مهمترین تمایز میان تجزیه پرتویی و فوتولیز (تخریب نوری)، در قدرت نفوذ و گزینشپذیری است. در فوتولیز، انرژی فوتونهای فرابنفش (UV) تنها توسط گروههای خاصی از اتمها که به آنها «کروموفور» میگوییم جذب میشود و معمولاً اثر آن محدود به لایههای سطحی قطعه است. اما در فرآیند رادیولیز، پرتوهای پرانرژی گاما یا الکترون، بدون توجه به ساختار شیمیایی، در تمام عمق قطعه نفوذ کرده و انرژی خود را به صورت تصادفی به هر الکترونی که در مسیرشان باشد منتقل میکنند. این یعنی ما در اینجا با یک پدیده حجمی روبرو هستیم، نه صرفاً یک پدیده سطحی.
تفاوت دیگر در مقایسه با ترمولیز (تخریب حرارتی) آشکار میشود. در تخریب حرارتی، انرژی به صورت گرما به کل سیستم داده میشود و باعث افزایش ارتعاشات مولکولی در تمام پیوندها میگردد تا زمانی که ضعیفترین پیوند بشکند. اما در رادیولیز، انرژی به صورت بستههای متمرکز و بسیار پرقدرت (شبیه به اصابت گلوله) به نقاط خاصی از مولکول برخورد میکند. این تمرکز انرژی باعث میشود که حتی قویترین پیوندها نیز بدون نیاز به افزایش دمای کلی قطعه، در کسری از ثانیه شکسته شوند و واکنشهایی را آغاز کنند که با دادن حرارت معمولی امکانپذیر نیستند.
مراحل زمانی رادیولیز
فرآیند رادیولیز یک رویداد لحظهای نیست، بلکه زنجیرهای از حوادث است که در مقیاسهای زمانی بسیار کوتاه آغاز شده و تا تغییرات شیمیایی پایدار ادامه مییابد. ما برای درک دقیق مکانیسم اثر پرتو بر پلیمر، این پدیده را به سه مرحله متمایز تقسیم میکنیم که هر کدام ویژگیهای ترمودینامیکی و سینتیکی خاص خود را دارند.
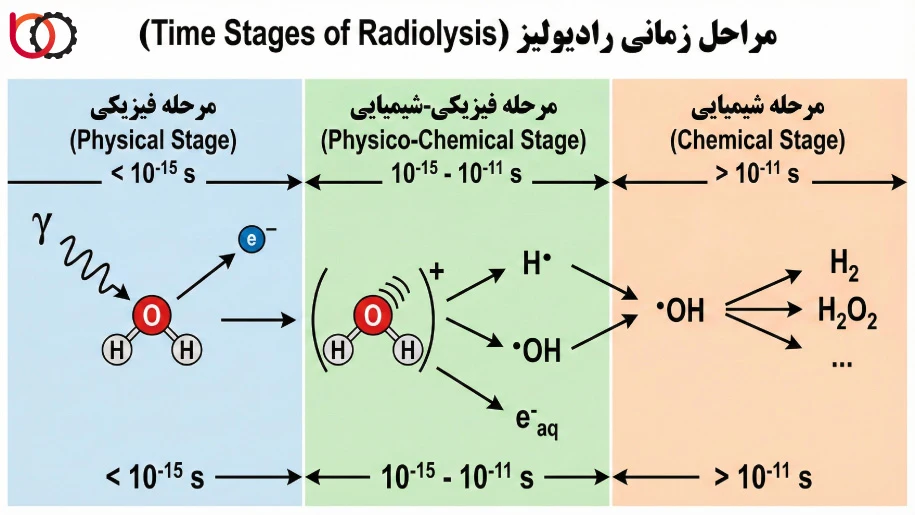
۱. مرحله فیزیکی (Physical Stage)
این نخستین فاز تعامل است که بسیار سریع رخ میدهد (تقریباً در بازه زمانی $10^{-18}$ تا $10^{-15}$ ثانیه). در این کسر ناچیز از ثانیه، ذره پرانرژی یا فوتون با الکترونهای مداری اتمهای پلیمر برخورد میکند. ما در این مرحله شاهد هیچ واکنش شیمیایی نیستیم؛ بلکه صرفاً انتقال انرژی صورت میگیرد. نتیجه این مرحله، تولید مولکولهای “برانگیخته” ($M^*$) و “یونیزه شده” ($M^+$) به همراه الکترونهای آزاد پرانرژی است. در واقع، سیستم انرژی را دریافت کرده اما هنوز فرصت واکنش نشان دادن به آن را پیدا نکرده است.
۲. مرحله فیزیکوشیمیایی (Physicochemical Stage)
بلافاصله پس از یونیزاسیون، سیستم وارد فاز فیزیکوشیمیایی میشود که حدوداً تا $10^{-6}$ ثانیه به طول میانجامد. در این بازه، گونههای ناپایدار تولید شده در مرحله قبل، تلاش میکنند تا انرژی اضافی خود را توزیع کنند. الکترونهای داغ (Hot Electrons) با برخورد به سایر مولکولها سرعت خود را از دست داده و به اصطلاح “ترمالیزه” میشوند. همچنین یونهای مثبت ممکن است با مولکولهای خنثی واکنش داده یا تجزیه شوند. مهمترین اتفاقی که ما در این مرحله رصد میکنیم، تبدیل یونها و مولکولهای برانگیخته به “رادیکالهای آزاد” است.
۳. مرحله شیمیایی (Chemical Stage)
پس از $10^{-6}$ ثانیه، مرحله شیمیایی آغاز میشود که میتواند از چند میکروثانیه تا ساعتها (یا حتی روزها در پلیمرهای نیمهکریستالی) ادامه یابد. در این فاز، رادیکالهای آزاد تولید شده که اکنون دارای طول عمر کافی هستند، شروع به نفوذ در ماتریس پلیمری میکنند. در اینجا است که واکنشهای اصلی تجزیه پرتویی مانند قطع زنجیر یا اتصال عرضی رخ میدهد. ما خروجی نهایی و تغییرات ملموس در خواص ماده را حاصل اتفاقاتی میدانیم که در این مرحله و از طریق واکنشهای رادیکالی تثبیت میشوند.
انتقال انرژی خطی (LET) در رادیولیز
در تحلیل فرآیند رادیولیز، تنها دانستن مقدار کل انرژی جذب شده (دوز) کافی نیست؛ بلکه نحوه توزیع این انرژی در فضای هندسی ماده نیز اهمیت حیاتی دارد. ما برای توصیف این توزیع از مفهومی به نام «انتقال انرژی خطی» یا LET (Linear Energy Transfer) استفاده میکنیم. این پارامتر نرخ انرژی سپردهگذاری شده توسط ذره باردار در طول مسیر عبور خود در ماده را نشان میدهد و معمولاً با واحد کیلو الکترونولت بر میکرومتر ($keV/\mu m$) بیان میشود:
$$LET = \frac{dE}{dx}$$
که در آن $dE$ تغییرات انرژی و $dx$ طول مسیر طی شده است.
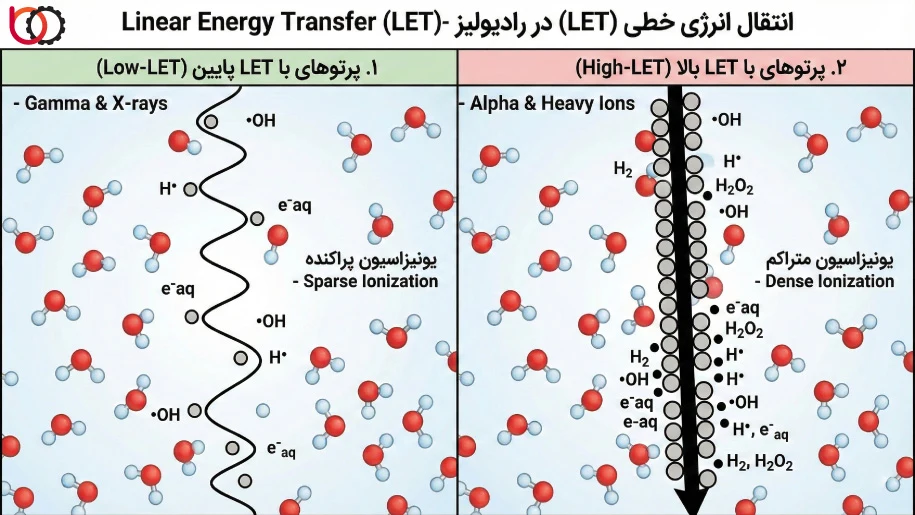
ما بر اساس مقدار LET، پرتوها را به دو دسته اصلی تقسیم میکنیم که رفتار تجزیه پرتویی متفاوتی در پلیمر ایجاد میکنند:
۱. پرتوهای با LET پایین (Low-LET)
پرتوهای گاما، ایکس و الکترونهای سریع (EB) در این دسته قرار میگیرند. این پرتوها انرژی خود را به صورت بستههای پراکنده و دور از هم در ماتریس پلیمر آزاد میکنند. فاصله بین رویدادهای یونیزاسیون در این حالت زیاد است. ما در کاربردهای صنعتی معمولاً از این نوع پرتوها استفاده میکنیم، زیرا پراکندگی رادیکالها اجازه میدهد تا آنها قبل از بازترکیب شدن با یکدیگر، با زنجیرههای پلیمری واکنش دهند و خواص مطلوب (مثل شبکهای شدن) را ایجاد کنند.
۲. پرتوهای با LET بالا (High-LET)
ذرات سنگین باردار مانند ذرات آلفا، پروتونها و یونهای سنگین دارای LET بالا هستند. این ذرات هنگام عبور از پلیمر، ستونی متراکم و پیوسته از یونها و رادیکالها را در مسیر خود ایجاد میکنند. در رادیولیز با LET بالا، غلظت موضعی رادیکالها در مسیر پرتو بسیار زیاد است. این تراکم باعث میشود احتمال برخورد رادیکالها با یکدیگر و خنثی شدن آنها (Recombination) بسیار بیشتر از احتمال واکنش آنها با زنجیره پلیمر باشد. به همین دلیل، بازده واکنشهای شیمیایی مفید در این حالت معمولاً کمتر است و تخریب موضعی شدیدتری رخ میدهد.
نظریه ردپا (Spur Theory) در توزیع انرژی
برای درک دقیقتر اتفاقاتی که در لحظه اولیه رادیولیز رخ میدهد، ما باید نگاهی عمیقتر از مفهوم LET داشته باشیم. اگرچه پرتوهای کمتراکم (Low-LET) مانند گاما و الکترون در مقیاس ماکروسکوپی انرژی را به صورت یکنواخت در کل حجم پلیمر پخش میکنند، اما در مقیاس نانومتری و مولکولی، توزیع انرژی کاملاً ناهمگن و گسسته است. نظریه ردپا یا Spur Theory مدلی است که ما برای توصیف این ناهمگونی میکروسکوپی از آن استفاده میکنیم.

طبق این نظریه، انرژی پرتو نه به صورت یک جریان پیوسته، بلکه به صورت بستهها یا خوشههایی مجزا از رویدادهای یونیزاسیون و برانگیختگی در طول مسیر حرکت ذره باردار آزاد میشود. ما این بستههای انرژی را بر اساس مقدار انرژی منتقل شده به سه دسته اصلی تقسیم میکنیم:
۱. ردپاها (Spurs)
رایجترین شکل انتقال انرژی در رادیولیز با پرتوهای گاما و الکترونی است. هر ردپا شامل انرژی کمتر از $100 eV$ است. ما تصور میکنیم که ردپاها شبیه به “دانههای تسبیح” در طول مسیر حرکت الکترون اولیه قرار دارند. در داخل هر ردپا، معمولاً ۱ تا ۳ جفت یون-الکترون یا رادیکال آزاد در فاصلهای بسیار نزدیک به هم حبس شدهاند.
۲. لکهها (Blobs)
اگر انرژی منتقل شده در یک ناحیه بین $100 eV$ تا $500 eV$ باشد، تراکم یونیزاسیون بیشتر شده و ساختاری بزرگتر به نام “لکه” ایجاد میشود. در اینجا همپوشانی ردپاها باعث میشود غلظت گونههای فعال بالاتر رود.
۳. مسیرهای کوتاه (Short Tracks)
زمانی که انرژی منتقل شده بین $500 eV$ تا $5 keV$ باشد، تراکم به قدری زیاد است که شبیه به یک مسیر استوانهای پیوسته از یونها میشود (شبیه به آنچه در پرتوهای آلفا میبینیم).
اهمیت این نظریه در شیمی رادیولیز پلیمر بسیار حیاتی است. سرنوشت رادیکالهای آزاد تشکیل شده در یک ردپا به رقابت بین دو پدیده بستگی دارد: «نفوذ به بیرون» و «بازترکیب». اگر رادیکالها بتوانند از محیط متراکم ردپا فرار کنند و در ماتریس پلیمر پخش شوند، واکنشهای مفید مثل شبکهای شدن را رقم میزنند. اما اگر در همان فضای بسته ردپا با هم برخورد کنند، یکدیگر را خنثی کرده و انرژی پرتو عملاً هدر میرود.
نقش الکترونهای ثانویه در فرآیند رادیولیز
در تحلیل دقیق سینتیک رادیولیز، ما با یک واقعیت جالب روبرو میشویم: بخش عمدهای از تغییرات شیمیایی که در پلیمر رخ میدهد، ناشی از برخورد مستقیم پرتو اولیه نیست، بلکه توسط «الکترونهای ثانویه» انجام میشود. زمانی که یک فوتون پرانرژی گاما یا یک ذره شتابدار اولیه با اتمی از زنجیره پلیمر برخورد میکند، باعث کنده شدن الکترون از مدار آن میشود. اگر این الکترونِ جدا شده انرژی جنبشی کافی داشته باشد، خودش به عنوان یک پرتابه جدید عمل کرده و میتواند یونیزاسیونهای بیشتری را رقم بزند.

ما در فیزیک پرتو به این الکترونهای پرانرژیِ تولید شده، الکترونهای ثانویه یا پرتوهای دلتا ($\delta$-rays) میگوییم. اهمیت آنها در فرآیند تجزیه پرتویی از آنجا ناشی میشود که پرتو اولیه معمولاً مسیر طولانیتری را طی میکند و برهمکنشهای پراکندهای دارد، اما الکترونهای ثانویه مسئول توزیع موضعی و متراکم انرژی هستند. در واقع، پرتو ورودی تنها نقش آغازگر را دارد و این لشکری از الکترونهای ثانویه است که انرژی را در بافت ماده پخش کرده و واکنشها را پیش میبرد.
سرنوشت این الکترونها در ماتریس پلیمری بسیار تعیینکننده است. آنها با حرکت در میان زنجیرهها و برخوردهای پیدرپی، انرژی خود را از دست داده و کُند میشوند تا به سطح انرژی حرارتی برسند (فرآیند Thermalization). ما در نهایت شاهد هستیم که این الکترونهای کُند شده (Thermalized Electrons) یا توسط حفرههای مثبت جذب شده و مولکولهای برانگیخته را میسازند (بازترکیب ژرمینال)، و یا در تلههای فیزیکی و شیمیایی پلیمر به دام افتاده و مراکز فعال واکنشدهنده را برای مراحل بعدی رادیولیز شیمیایی ایجاد میکنند.
مکانیزم تشکیل رادیکالهای آزاد پلیمری
در فرآیند رادیولیز پلیمر، مرحله اصلی تبدیل انرژی جذب شده به تغییرات شیمیایی، «تشکیل رادیکال آزاد» است. ما رادیکال را اتم یا مولکولی تعریف میکنیم که دارای یک یا چند الکترون جفتنشده در اوربیتال لایه ظرفیت خود باشد. وجود این الکترون جفتنشده باعث ناپایداری شدید شده و گونه شیمیایی را به سمت واکنشهای سریع برای رسیدن به آرایش الکترونی پایدار سوق میدهد. در واقع، تمام تغییرات نهایی در خواص فیزیکی و مکانیکی قطعه، ناشی از واکنشپذیری همین رادیکالهای اولیه است.
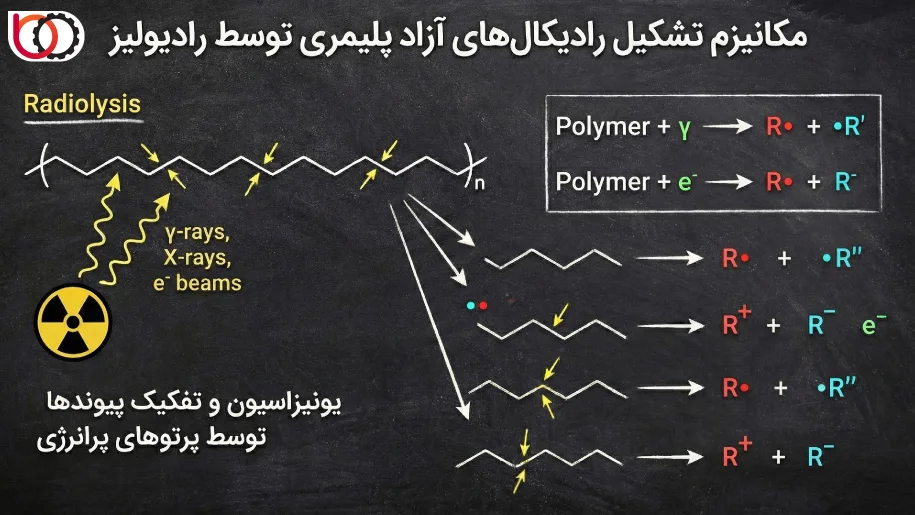
مکانیزم غالب تولید این گونهها در اثر تابش، از طریق شکست پیوند در مولکولهای برانگیخته (Excited States) صورت میگیرد. زمانی که زنجیره پلیمری انرژی پرتو را دریافت میکند و به سطح انرژی بالاتر ($P^*$) میرود، پیوندهای کووالانسی آن (عمدتاً پیوندهای جانبی $C-H$ یا پیوندهای اسکلتی $C-C$) دچار ناپایداری میشوند. اگر انرژی دریافتی از انرژی تفکیک پیوند فراتر رود، شکست پیوند رخ میدهد. ما این شکست را معمولاً از نوع «همولیتیک» (Homolytic) میدانیم؛ بدین معنا که جفت الکترون اشتراکی تقسیم شده و هر اتم با یک الکترون جدا میشود:
$$R-H \xrightarrow{\gamma / e^-} R^\bullet + H^\bullet$$
در رابطه بالا، $R^\bullet$ نشاندهنده «ماکرورادیکال» است که روی زنجیره اصلی پلیمر باقی میماند و $H^\bullet$ اتم هیدروژن رادیکالی است که متحرک بوده و میتواند در ماتریس پلیمر نفوذ کند.
مسیر دومی که ما در نظر میگیریم، واکنشهای کاتیونی و آنیونی است. یونهای پلیمری ($P^+$) که در فاز فیزیکی ایجاد شدهاند، اغلب ناپایدار هستند و سریعاً وارد برهمکنش با مولکولهای خنثی مجاور میشوند. برای نمونه، فرآیند انتقال پروتون یا خنثی شدن بار الکتریکی توسط الکترونهای حرارتی، در نهایت منجر به تولید رادیکالهای خنثی میشود. بنابراین، چه از مسیر برانگیختگی مستقیم و چه از مسیر واکنشهای یونی، نتیجه فرآیند تجزیه پرتویی، ایجاد مراکز فعال شیمیایی متعدد در ساختار پلیمر است.
انواع رادیکالهای ماکرومولکولی
در بررسیهای شیمی رادیولیز، این نکته آشکار میشود که موقعیت قرارگیری الکترون منفرد روی زنجیره پلیمری، نقشی تعیینکننده در رفتار بعدی آن دارد. همه رادیکالها عملکرد یکسانی ندارند؛ واکنشپذیری، طول عمر و نوع محصول نهایی (تخریب یا شبکهای شدن) مستقیماً به ساختار شیمیایی و محل تشکیل رادیکال وابسته است. این گونههای فعال پلیمری را که «ماکرورادیکال» نامیده میشوند، بر اساس موقعیت هندسی و پایداری الکترونی به سه دسته اصلی تقسیم میکنیم.
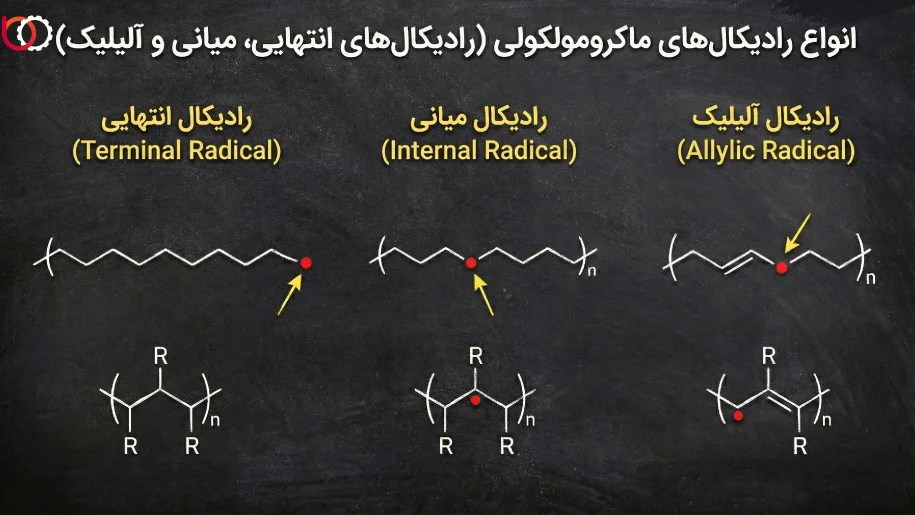
۱. رادیکالهای انتهایی (Terminal Radicals)
این نوع رادیکال زمانی ایجاد میشود که پیوند کووالانسی کربن-کربن ($C-C$) در اسکلت اصلی پلیمر بشکند. این پدیده معمولاً نتیجه مستقیم قطع زنجیر در نظر گرفته میشود. وقتی زنجیره اصلی دو نیم میشود، دو رادیکال در محل شکستگی (انتهای زنجیرههای جدید) شکل میگیرند:
$$-CH_2-CH_2-CH_2- \xrightarrow{Energy} -CH_2-CH_2^\bullet + ^\bullet CH_2-$$
رادیکالهای انتهایی معمولاً تحرکپذیری بالایی دارند (چون در انتهای زنجیر آزاد هستند) و اغلب پیشمادهای برای واکنشهای دپلیمریزاسیون (Depolymerization) یا بازترکیب نامطلوب محسوب میشوند. در فرآیندهای تخریبی تجزیه پرتویی، حضور این گونهها غالب است.
۲. رادیکالهای میانی (Mid-chain Radicals)
این گونهها حاصل جدا شدن یک اتم جانبی (معمولاً هیدروژن) از بدنه اصلی زنجیره هستند، بدون اینکه پیوستگی اسکلت کربنی قطع شود. به این فرآیند «انتزاع هیدروژن» (Hydrogen Abstraction) گفته میشود:
$$-CH_2-CH_2-CH_2- \xrightarrow{Energy} -CH_2-\dot{C}H-CH_2- + H^\bullet$$
رادیکالهای میانی اهمیت صنعتی بسیار بالایی دارند. از آنجا که این رادیکالها در وسط زنجیره قرار دارند، اگر دو زنجیره حاوی رادیکال میانی به هم نزدیک شوند، میتوانند با یکدیگر پیوند برقرار کرده و ساختار شبکهای (Cross-link) ایجاد کنند. بنابراین، رادیکالهای میانی عامل اصلی بهبود خواص حرارتی و مکانیکی در پلیمرهایی مثل پلیاتیلن شناخته میشوند.
۳. رادیکالهای آلیلیک (Allylic Radicals)
در پلیمرهایی که دارای پیوندهای دوگانه کربن-کربن هستند (مانند لاستیکهای غیراشباع)، نوع سوم و پایدارتری از رادیکالها شکل میگیرد. اگر الکترون منفرد روی کربنی تشکیل شود که در همسایگی یک پیوند دوگانه قرار دارد، پدیده رزونانس رخ میدهد:
$$-CH=CH-\dot{C}H- \longleftrightarrow -\dot{C}H-CH=CH-$$
این رزونانس باعث پایداری نسبی رادیکال میشود. در آزمایشها مشاهده میشود که رادیکالهای آلیلیک طول عمر بیشتری نسبت به رادیکالهای آلکیل معمولی دارند و دیرتر از بین میروند. این پایداری باعث میشود که این رادیکالها تا مدتها پس از قطع تابش در ساختار باقی بمانند و به مرور زمان با اکسیژن محیط واکنش داده و منجر به اکسیداسیون تدریجی قطعه شوند.
این بخش به بررسی یکی از مهمترین پدیدههای دینامیک در شیمی پلیمر میپردازد که عامل اصلی جابجایی مراکز واکنش در طول ماده است:
واکنشهای انتقال هیدروژن در زنجیره پلیمر
در فرآیند رادیولیز، مکان اولیهای که رادیکال آزاد در آن تشکیل میشود، لزوماً مکان نهایی واکنش نیست. رادیکالهای پلیمری، بهویژه در دماهای بالاتر از دمای انتقال شیشهای ($T_g$)، قابلیت تحرک و جابجایی مراکز فعال خود را دارند. این مهاجرت شیمیایی اغلب از طریق مکانیزمی به نام «انتقال هیدروژن» (Hydrogen Transfer) یا «انتزاع هیدروژن» صورت میگیرد. در این فرآیند، یک رادیکال فعال ($R^\bullet$) به پیوند $C-H$ در همسایگی خود حمله کرده و اتم هیدروژن را میرباید. نتیجه این تبادل، اشباع شدن رادیکال اولیه و تشکیل یک رادیکال جدید در مکان دوم است:
$$R_1^\bullet + R_2-H \longrightarrow R_1-H + R_2^\bullet$$
این واکنش از نظر ترمودینامیکی معمولاً در جهتی پیش میرود که رادیکال پایدارتر ایجاد شود. برای مثال، اگر یک رادیکال اولیه (روی کربن انتهای زنجیر) بتواند با گرفتن هیدروژن از یک کربن ثالثیه (Tertiary Carbon) در وسط زنجیر، مرکز فعال را به نقطهای با ممانعت فضایی بیشتر و پایداری بالاتر منتقل کند، این اتفاق به سرعت رخ میدهد.
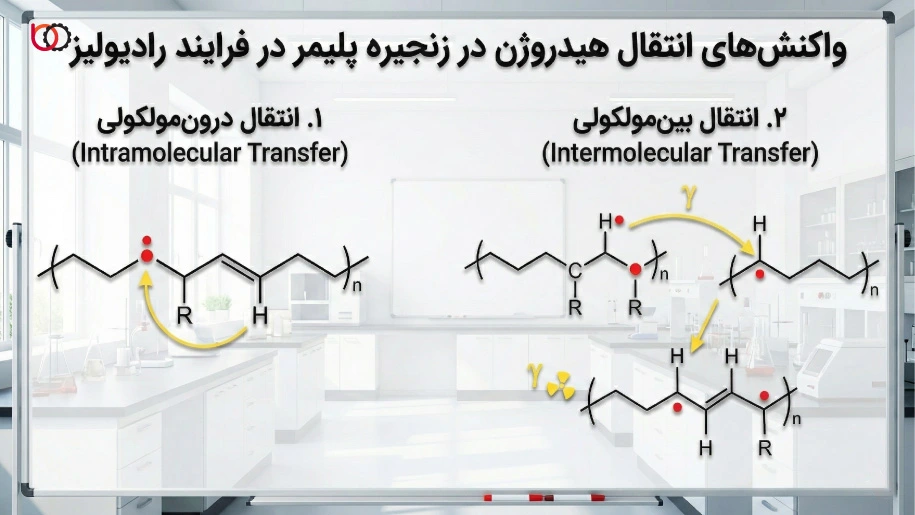
انتقال هیدروژن به دو صورت کلی در ماتریس پلیمر مشاهده میشود:
۱. انتقال درونمولکولی (Intramolecular Transfer)
در این حالت، رادیکال موجود روی زنجیره به سمت عقب برمیگردد و هیدروژنی را از همان زنجیره خودش جدا میکند. این پدیده که به «Backbiting» معروف است، باعث میشود مرکز واکنش در طول همان زنجیره حرکت کند. این جابجایی برای رسیدن رادیکالها به نقاطی که مستعد قطع زنجیر هستند (مانند کربنهای نوع چهارم) حیاتی است.
۲. انتقال بینمولکولی (Intermolecular Transfer)
در اینجا، رادیکال یک زنجیره با زنجیره مجاور برهمکنش میدهد. این نوع انتقال اهمیت ویژهای در فرآیند شبکهای شدن (Cross-linking) دارد. برای اینکه دو زنجیره بتوانند به هم متصل شوند، نیاز است که دو رادیکال در فاصلهای بسیار نزدیک به هم قرار بگیرند. انتقال بینمولکولی هیدروژن این امکان را فراهم میکند که مراکز فعال روی زنجیرههای همسایه “جستوجو” کنند تا در موقعیت هندسی مناسب برای تشکیل پیوند کووالانسی $C-C$ بین دو زنجیره قرار گیرند.
بدون وقوع واکنشهای انتقال هیدروژن، بسیاری از فرآیندهای اصلاحی رادیولیز متوقف میشدند، زیرا رادیکالهای اولیه اغلب در قفسهای پلیمری (Polymer Cages) به دام افتاده و امکان دسترسی به یکدیگر را نداشتند.
مکانیزم دقیق قطع زنجیر (Chain Scission)
در مقابل فرآیند شبکهای شدن که منجر به افزایش وزن مولکولی میشود، قطع زنجیر (Chain Scission) یا تخریب (Degradation)، پدیدهای است که در آن اسکلت اصلی پلیمر شکسته شده و طول زنجیرهها کاهش مییابد. در رادیولیز، این اتفاق منجر به کاهش شدید میانگین وزن مولکولی ($M_w$) میشود و خواص مکانیکی پلیمر را به سمت شکنندگی و از دست دادن استحکام سوق میدهد. در این حالت، انرژی پرتو به جای ایجاد اتصالات جدید، صرف غلبه بر انرژی پیوند کووالانسی کربن-کربن ($C-C$) در ستون فقرات پلیمر میشود.
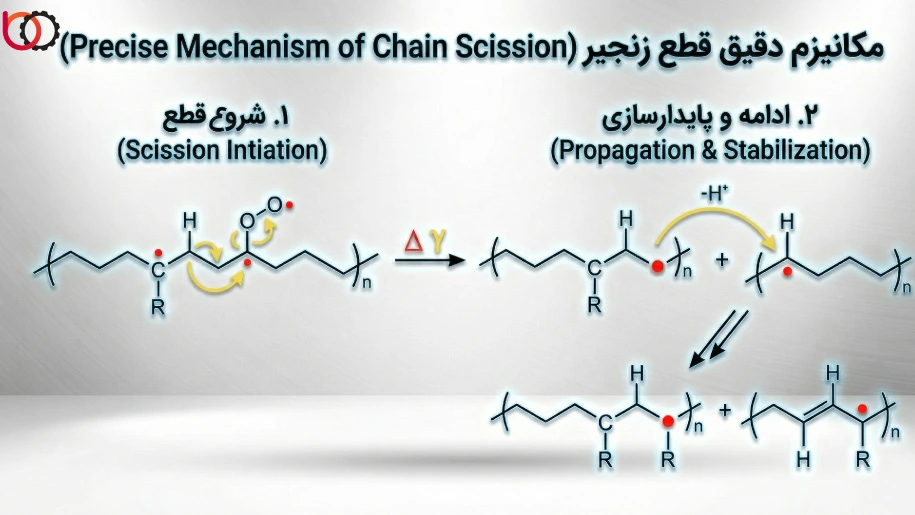
مکانیزم شیمیایی غالب در قطع زنجیر، فرآیندی است که به «شکست بتا» ($\beta$-scission) معروف است. این واکنش معمولاً زمانی رخ میدهد که یک رادیکال آزاد روی زنجیره اصلی تشکیل شود، اما به دلیل ممانعت فضایی یا پایداری ترمودینامیکی، امکان انتقال هیدروژن یا اتصال به زنجیره دیگر را نداشته باشد. در این شرایط، الکترون منفرد باعث ناپایداری پیوند کربن-کربن در موقعیت بتا (نسبت به مرکز رادیکالی) میشود و زنجیره به دو قسمت تقسیم میگردد: یک زنجیره با انتهای غیراشباع (پیوند دوگانه) و یک زنجیره با انتهای رادیکالی جدید.
$$-CH_2-C(R)(CH_3)-CH_2- \xrightarrow{Radiation} -CH_2-C(CH_3)=CH_2 + ^\bullet C(R)-$$
ساختار شیمیایی واحد تکرارشونده (Monomer Unit) تعیینکننده اصلی در وقوع این پدیده است. قاعده کلی در رادیولیز پلیمرها نشان میدهد که اگر در واحد تکرارشونده، اتم کربن نوع چهارم (کربنی که به چهار گروه غیر هیدروژنی متصل است) وجود داشته باشد، احتمال قطع زنجیر بسیار بالا میرود. دلیل این امر، ممانعت فضایی گروههای جانبی است که اجازه نزدیک شدن زنجیرهها برای شبکهای شدن را نمیدهد و همچنین پایداری پایین پیوند $C-C$ در این نقاط پرتنش است. پلیمرهایی مانند پلیمتیلمتاکریلات (PMMA)، پلیایزوبوتیلن (PIB) و پلیتترافلوئورواتیلن (PTFE) از جمله موادی هستند که در برابر پرتو، رفتار غالبِ قطع زنجیر را از خود نشان میدهند و به جای سخت شدن، نرم یا پودر میشوند.
برای کمیسازی این پدیده، از پارامتری به نام $G(S)$ استفاده میشود که نشاندهنده تعداد شکستهای زنجیره اصلی به ازای هر $100 eV$ انرژی جذب شده است. بالا بودن مقدار $G(S)$ نسبت به $G(X)$ (بازده شبکهای شدن)، نشاندهنده حساسیت ذاتی پلیمر به تخریب پرتویی است.
مکانیزم دقیق شبکهای شدن (Cross-linking)
در نقطه مقابل پدیده تخریب، فرآیند شبکهای شدن یا اتصال عرضی قرار دارد. این پدیده مطلوبترین اتفاق در صنعت فرآورش تابشی است، زیرا ساختار خطی و ضعیف پلیمرهای ترموپلاستیک را به ساختاری سهبعدی، مستحکم و مقاوم در برابر حرارت (شبیه به ترموستها) تبدیل میکند. در طی این فرآیند، انرژی پرتو باعث میشود که بین زنجیرههای مجاور پلیمر، پیوندهای کووالانسی جدید برقرار شود و عملاً تمام قطعه به یک مولکول واحد و غولپیکر تبدیل گردد.
مکانیزم شیمیایی غالب در شبکهای شدن ناشی از رادیولیز، واکنش «بازترکیب رادیکالها» (Recombination) است. زمانی که دو ماکرورادیکال که روی زنجیرههای همسایه قرار دارند، در اثر نفوذ و جابجایی به فاصله پیوندی مناسب (حدود چند آنگستروم) از یکدیگر میرسند، الکترونهای منفرد آنها با هم جفت شده و یک پیوند کربن-کربن بینزنجیری تشکیل میدهند. رایجترین نوع این اتصال، تشکیل ساختار H-شکل (H-type Crosslink) است:
$$-CH_2-\dot{C}H-CH_2- \quad + \quad -CH_2-\dot{C}H-CH_2- \longrightarrow \begin{matrix} -CH_2-CH-CH_2- \\ | \\ -CH_2-CH-CH_2- \end{matrix}$$
علاوه بر بازترکیب مستقیم، مسیر دیگری به نام «اتصال Y-شکل» نیز وجود دارد که در آن یک رادیکال پلیمری به یک پیوند دوگانه (C=C) موجود در زنجیره دیگر حمله میکند. این نوع اتصال معمولاً در پلیمرهایی که دارای گروههای غیراشباع وینیل هستند یا در حین تابش دچار تشکیل پیوند دوگانه شدهاند، مشاهده میشود.
شاخص کمی سنجش این فرآیند، مقدار $G(X)$ است که نشان میدهد به ازای هر $100 eV$ انرژی جذب شده، چند اتصال عرضی ایجاد شده است. شرط لازم برای اینکه یک پلیمر در نهایت شبکهای شود و به نقطه ژل (Gel Point) برسد، این است که نرخ شبکهای شدن بر نرخ قطع زنجیر غلبه کند (معمولاً نسبت $G(X) > 4 G(S)$). پلیاتیلن (PE) بارزترین نمونه پلیمری است که به دلیل ساختار ساده و فقدان گروههای حجیم، تمایل شدیدی به شبکهای شدن تحت تابش دارد و خواص حرارتی آن پس از تابش به طرز چشمگیری بهبود مییابد.
اثر قفس (Cage Effect) در بازترکیب رادیکالها
در تحلیل سینتیک واکنشهای رادیولیز، همواره این سوال مطرح میشود که چرا مقدار محصولات شیمیایی نهایی اغلب کمتر از تعداد رادیکالهای اولیه تولید شده است؟ پاسخ در پدیدهای فیزیکی به نام «اثر قفس» نهفته است. زمانی که یک پیوند شیمیایی در اثر جذب انرژی میشکند و دو رادیکال تولید میکند، این رادیکالها در فضای خلأ قرار ندارند؛ بلکه توسط دیواری متراکم از سایر زنجیرههای پلیمری احاطه شدهاند. این محیط ویسکوز و فشرده مانند یک قفس عمل کرده و مانع از دور شدن سریع رادیکالها از یکدیگر میشود.
در فاز جامد پلیمری، به دلیل تحرک پایین مولکولی، رادیکالهای دوقلو (Geminate Radicals) که از یک مولکول مادر متولد شدهاند، برای مدت کوتاهی در کنار هم حبس میشوند. در این وضعیت، احتمال برخورد مجدد آنها با یکدیگر بسیار بالا است. اگر این برخورد منجر به تشکیل دوباره پیوند اولیه شود، انرژی جذب شده عملاً به صورت گرما تلف شده و هیچ تغییر شیمیایی پایداری در ساختار پلیمر ثبت نمیشود. به این فرآیند «بازترکیب ژرمینال» (Geminate Recombination) گفته میشود.
اثر قفس باعث میشود که بازده کوانتومی واکنشهای رادیولیز در جامدات بسیار کمتر از فاز مایع یا گاز باشد. تنها آن دسته از رادیکالهایی میتوانند در فرآیندهای مفیدی مثل شبکهای شدن شرکت کنند که انرژی جنبشی کافی برای “فرار از قفس” را داشته باشند و بتوانند در ماتریس پلیمر نفوذ کنند. بنابراین، عواملی مانند “حجم آزاد” (Free Volume) پلیمر و دمای محیط که بر نفوذپذیری و نرمی زنجیرهها اثر میگذارند، مستقیماً بر شانس فرار رادیکالها و در نتیجه بر راندمان نهایی فرآیند تاثیرگذار هستند.
تشکیل پیوندهای غیراشباع و تغییر رنگ پلیمر
یکی از پدیدههای رایج که همزمان با قطع زنجیر یا شبکهای شدن در فرآیند رادیولیز مشاهده میشود، تشکیل گروههای غیراشباع یا پیوندهای دوگانه ($C=C$) در ساختار پلیمر است. این اتفاق معمولاً زمانی رخ میدهد که دو اتم یا گروه جانبی از روی دو کربن همسایه حذف شوند. برای مثال، در پلیاتیلن، خروج مولکول هیدروژن ($H_2$) منجر به تشکیل پیوند دوگانه وینیلن در طول زنجیره میشود:
$$-CH_2-CH_2- \xrightarrow{Radiation} -CH=CH- + H_2$$
اگر این حذف گروهها در چندین واحد تکرارشونده پشت سر هم اتفاق بیفتد، سیستمهای مزدوج (Conjugated Systems) یا پلینها شکل میگیرند. در پلیمرهایی مانند PVC، خروج هیدروکلریک اسید ($HCl$) تحت تابش، منجر به تشکیل توالی طولانی از پیوندهای دوگانه میشود که پایداری شیمیایی ماده را به شدت تحت تاثیر قرار میدهد.

پیامد مستقیم تشکیل این ساختارهای غیراشباع و به دام افتادن رادیکالها، تغییر رنگ پلیمر است. در حالت عادی، بسیاری از پلیمرها شفاف یا سفید هستند زیرا در ناحیه مرئی طیف نوری جذب ندارند. اما پیوندهای دوگانه مزدوج و برخی رادیکالهای به دام افتاده، به عنوان مراکز رنگساز (Chromophores) عمل میکنند. این مراکز با جذب طول موجهای خاصی از نور مرئی (معمولاً در ناحیه آبی)، باعث میشوند که پلیمر بازتابی متمایل به زرد یا قهوه ای داشته باشد.
پدیده «زرد شدن» (Yellowing) یکی از چالشهای اصلی در استریلیزاسیون تجهیزات پزشکی با پرتو گاما است. شدت این تغییر رنگ به دوز تابش، نوع پلیمر و حضور پایدارکنندهها بستگی دارد. اگرچه در برخی موارد این تغییر رنگ با گذشت زمان و نفوذ اکسیژن (که با رادیکالهای رنگساز واکنش میدهد) کاهش مییابد و اصطلاحاً رنگبری (Bleaching) رخ میدهد، اما معمولاً به عنوان نشانهای بصری از تغییرات شیمیایی عمیق در اثر رادیولیز در نظر گرفته میشود.
تولید گازهای رادیولیتیک در پلیمرها ($H_2$, $CO$, $CO_2$, $CH_4$)
یکی از نتایج اجتنابناپذیر برهمکنش پرتوهای یونساز با مواد آلی، آزاد شدن مولکولهای کوچک و فرار گازی است. در حین فرآیند رادیولیز، زمانی که پیوندهای جانبی یا اصلی پلیمر میشکنند، اتمها و گروههای جدا شده همیشه دوباره به زنجیره متصل نمیشوند؛ بلکه اغلب با یکدیگر ترکیب شده و گازهایی را تشکیل میدهند که از ماتریس پلیمر خارج میشوند. نوع و مقدار این گازها مانند «اثر انگشت» شیمیایی عمل کرده و اطلاعات دقیقی درباره ساختار پلیمر و مکانیزم تخریب آن ارائه میدهد.
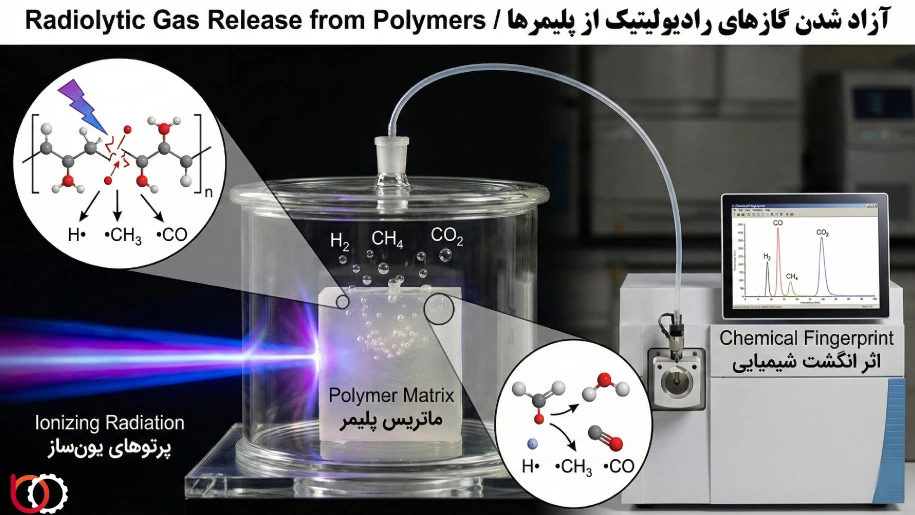
۱. هیدروژن ($H_2$)
هیدروژن تقریباً در تمام پلیمرهای آلی، اصلیترین گاز تولید شده است. علت این امر فراوانی پیوندهای $C-H$ در ساختار پلیمرها و انرژی پیوندی نسبتاً پایین آنها در مقایسه با سایر گروهها است. خروج هیدروژن معمولاً نشانه وقوع واکنشهای شبکهای شدن یا تشکیل پیوندهای غیراشباع است. در پلیاتیلن، بیش از ۹۰ درصد کل گازهای خروجی را هیدروژن تشکیل میدهد.
۲. متان ($CH_4$) و هیدروکربنهای سبک
اگر پلیمر دارای شاخههای جانبی کوتاه باشد (مانند گروه متیل در پلیپروپیلن یا PMMA)، شکستن پیوند این گروهها منجر به تولید متان یا سایر آلکانهای سبک میشود. حضور این گازها نشاندهنده تخریب شاخههای جانبی است که میتواند بر خواص بلورینگی و مکانیکی ماده اثر بگذارد.
۳. مونوکسید و دیاکسید کربن ($CO$, $CO_2$)
در پلیمرهایی که دارای اتم اکسیژن در ساختار خود هستند (مانند پلیاسترها، پلیکربناتها یا سلولز)، شکستن گروههای عاملی استری یا کربونیل منجر به آزاد شدن $CO$ و $CO_2$ میشود. همچنین، اگر تابشدهی در محیط هوا انجام شود، واکنش رادیکالهای سطحی با اکسیژن محیط (اکسیداسیون پرتویی) نیز منبع مهمی برای تولید $CO_2$ است.
شناخت و کنترل این گازها از نظر ایمنی صنعتی بسیار حیاتی است. تجمع هیدروژن و متان در بستهبندیهای مهر و موم شده محصولات پلیمری پرت دیده، میتواند منجر به باد کردن بستهبندی یا حتی ایجاد خطر انفجار شود. به همین دلیل، در طراحی فرآیندهای استریلیزاسیون و انبارداری قطعات پلیمری، نرخ تولید گازهای رادیولیتیک (G-value of gas) همواره به عنوان یک پارامتر کلیدی محاسبه و لحاظ میشود.
روشهای آنالیز تغییرات ناشی از رادیولیز
برای درک اینکه یک پلیمر پس از تابشدهی چه سرنوشتی پیدا کرده است، مشاهده ظاهری کافی نیست. تغییرات اصلی در مقیاس آنگستروم و نانومتر رخ میدهند. ما برای ردیابی این تغییرات، از مجموعهای از تکنیکهای طیفسنجی، حرارتی و میکروسکوپی استفاده میکنیم که هر کدام قطعهای از پازل رادیولیز را تکمیل میکنند. انتخاب روش صحیح آنالیز، به نوع اطلاعات مورد نیاز (شیمیایی، ساختاری یا مورفولوژیکی) بستگی دارد.
کاربرد رزونانس اسپین الکترون (ESR) در شناسایی رادیکالها
مستقیمترین و قدرتمندترین روش برای اثبات وقوع رادیولیز، استفاده از طیفسنجی «رزونانس اسپین الکترون» (Electron Spin Resonance) یا EPR است. از آنجا که رادیکالهای آزاد دارای الکترون جفتنشده هستند، دارای ممان مغناطیسی بوده و در میدان مغناطیسی خارجی رفتار خاصی نشان میدهند. دستگاه ESR تنها تکنیکی است که قادر است به طور اختصاصی این گونههای پارامغناطیس را “ببیند”.
ما در آنالیز ESR، نمونه پلیمری را (معمولاً در دمای کرایوژنیک یا نیتروژن مایع) تحت تابش قرار داده و سپس در میدان مغناطیسی دستگاه قرار میدهیم. الگوی سیگنالهای دریافتی، نوع دقیق رادیکال (آلکیل، آلیل، پراکسی و…) را مشخص میکند. همچنین با بررسی شدت سیگنال در گذر زمان یا با افزایش دما، سینتیک زوال رادیکالها (Radical Decay) محاسبه میشود. این اطلاعات برای تخمین طول عمر رادیکالهای به دام افتاده که عامل اصلی پیرشدگی پلیمر در درازمدت هستند، حیاتی است.
آنالیز طیفسنجی مادون قرمز (FTIR) برای تغییرات ساختاری
برای رصد تغییرات در گروههای عاملی شیمیایی، طیفسنجی تبدیل فوریه مادون قرمز (FTIR) ابزار استاندارد آزمایشگاهی است. در فرآیند رادیولیز، پیوندهای شیمیایی شکسته شده و پیوندهای جدیدی شکل میگیرند که هر کدام فرکانس ارتعاشی متفاوتی در ناحیه مادون قرمز دارند. ما با مقایسه طیف نمونه شاهد (تابش ندیده) و نمونه پرتودهی شده، تغییرات شیمیایی را به صورت کمی و کیفی تحلیل میکنیم.
دو ناحیه در طیف FTIR اهمیت ویژهای در بحث تجزیه پرتویی دارند:
- ۱. ناحیه کربونیل ($1700-1750 cm^{-1}$): ظهور پیک در این ناحیه نشاندهنده اکسیداسیون پلیمر در حین تابش (تشکیل کتون، آلدهید یا اسید) است.
- ۲. ناحیه غیراشباع ($900-1000 cm^{-1}$ و $1600-1650 cm^{-1}$): تشکیل پیوندهای دوگانه وینیل یا ترانس-وینیلن که ناشی از حذف هیدروژن است، در این نواحی ظاهر میشود. همچنین کاهش شدت پیکهای مربوط به گروههای خاص، میزان تخریب آن گروهها را نشان میدهد.
استفاده از کروماتوگرافی گازی (GC) برای تحلیل گازهای خروجی
همانطور که پیشتر اشاره شد، خروج گاز نشانه قطعی تغییر ساختار است. برای شناسایی دقیق جنس و مقدار این گازها، از تکنیک «کروماتوگرافی گازی» (Gas Chromatography) استفاده میشود. در این روش، نمونه پلیمر در یک محفظه بسته (Vial) تحت تابش قرار میگیرد (Headspace Analysis) و سپس گازهای تجمع یافته در فضای بالای ظرف به دستگاه GC تزریق میشوند.
تحلیل نسبت گازها به ما کمک میکند تا مکانیزم غالب را کشف کنیم. برای مثال، اگر در آنالیز یک پلیاولفین، نسبت متان به هیدروژن افزایش یابد، نشاندهنده وقوع شکست در شاخههای جانبی است. همچنین وجود گازهایی مانند $CO$ و $CO_2$ در پلیمرهای اکسیژندار، شاهدی بر شکست زنجیره از محل گروههای عاملی حساس است. محاسبه “مقدار G تشکیل گاز” ($G_{gas}$) دقیقا از طریق همین دادههای GC انجام میشود.
اندازهگیری تغییرات وزن مولکولی با ویسکومتری
تغییر در اندازه زنجیرههای پلیمری، ملموسترین اثر فیزیکی رادیولیز است. ویسکومتری (Viscometry) روشی ساده اما دقیق برای پایش این تغییرات است. ویسکوزیته ذاتی یک محلول پلیمری طبق رابطه مارک-هاوینک (Mark-Houwink) با وزن مولکولی متوسط وزنی ($M_w$) رابطه مستقیم دارد:
$$[\eta] = K M_v^\alpha$$
اگر فرآیند غالب در تجزیه پرتویی، قطع زنجیر باشد، ویسکوزیته محلول پلیمری پس از تابش کاهش مییابد. اما اگر شبکهای شدن رخ دهد، ویسکوزیته افزایش یافته و در نهایت با رسیدن به نقطه ژل، بخشی از پلیمر نامحلول میشود. در این مرحله، ما با انجام آزمایش «استخراج سل-ژل» (Sol-Gel Extraction) و توزین بخش نامحلول، درصد شبکهای شدن را به صورت کمی محاسبه میکنیم که معیار اصلی کنترل کیفیت در صنایعی مانند تولید کابل و لوله است.
بررسی تغییرات خواص حرارتی با DSC و TGA
تغییرات ساختاری ناشی از پرتو، مستقیماً بر رفتار حرارتی ماده اثر میگذارند. کالریمتری روبشی تفاضلی (DSC) برای اندازهگیری دمای ذوب ($T_m$) و دمای انتقال شیشهای ($T_g$) استفاده میشود. در فرآیند شبکهای شدن، به دلیل محدود شدن حرکت زنجیرهها، معمولاً $T_g$ افزایش مییابد، در حالی که $T_m$ و درجه کریستالینیتی ممکن است کاهش یابند (زیرا اتصالات عرضی مانع از آرایش منظم بلورها میشوند).
از طرف دیگر، آنالیز توزین حرارتی (TGA) پایداری حرارتی ماده را میسنجد. نمودارهای TGA نشان میدهند که پلیمر پرتودهی شده در چه دمایی شروع به تجزیه شدن میکند. معمولاً پلیمرهای شبکهای شده پایداری حرارتی بالاتری نسبت به نمونه خام دارند، در حالی که پلیمرهای تخریب شده (Chain Scission) در دماهای پایینتری دچار افت وزن میشوند. این دادهها برای پیشبینی عمر سرویسدهی قطعه حیاتی هستند.
آنالیز تغییرات سطح پلیمر با میکروسکوپ الکترونی (SEM)
در دوزهای بالای تابش، اثرات رادیولیز میتواند به سطح ماکروسکوپی رسیده و باعث ایجاد ترکهای ریز، حفرهها و تغییر در زبری سطح شود. میکروسکوپ الکترونی روبشی (SEM) به ما اجازه میدهد تا توپوگرافی سطح را با بزرگنمایی بالا مشاهده کنیم.
در کامپوزیتهای پلیمری، SEM میتواند جدایش فازها یا شکست در فصلمشترک الیاف و ماتریس را که ناشی از تخریب پرتویی است، آشکار کند. همچنین در کاربردهایی مثل “Track Etching” (که در ساخت فیلترهای دقیق استفاده میشود)، از SEM برای مشاهده و اندازهگیری قطر منافذی که پس از اچ کردن شیمیاییِ مسیرهای تخریب شده پرتویی ایجاد شدهاند، استفاده میشود. این تصاویر دیداری، مکمل دادههای طیفسنجی بوده و درک فیزیکی عمیقی از شدت تخریب سطحی ارائه میدهند.
تاثیر متغیرهای محیطی بر رادیولیز
واکنشهای شیمیایی ناشی از پرتو، در خلأ اتفاق نمیافتند. اگرچه انرژی اولیه توسط ساختار پلیمر جذب میشود، اما مسیری که این انرژی تا رسیدن به محصولات نهایی طی میکند، شدیداً تحت تاثیر محیط اطراف و شرایط فیزیکی ماده است. در بسیاری از موارد، اهمیت عوامل محیطی مانند اکسیژن، دما و فاز فیزیکی ماده، برابر با اهمیت ساختار شیمیایی خودِ پلیمر است. مهندسین پلیمر با کنترل این متغیرها، شدت رادیولیز را تنظیم کرده و آن را به سمت هدف مورد نظر (تخریب یا اصلاح) هدایت میکنند.
رادیولیز اکسایشی (تاثیر اکسیژن و نفوذپذیری)
حضور اکسیژن در محیط تابشدهی، مخربترین عامل برای فرآیندهای اصلاحی و قویترین کاتالیزور برای فرآیندهای تخریبی است. زمانی که تابشدهی در مجاورت هوا انجام میشود، اکسیژن به دلیل خاصیت پارامغناطیسی خود، با سرعتی بسیار بالا (بسیار سریعتر از واکنشهای شبکهای شدن) با رادیکالهای پلیمری ($R^\bullet$) واکنش داده و «رادیکالهای پراکسی» ($ROO^\bullet$) را تشکیل میدهد:
$$R^\bullet + O_2 \longrightarrow ROO^\bullet$$
این واکنش آغازگر زنجیرهای از اتفاقات مخرب است که به آن «رادیولیز اکسایشی» میگویند. رادیکال پراکسی با جذب هیدروژن از زنجیره مجاور، به هیدروپراکسید ناپایدار ($ROOH$) تبدیل میشود که در نهایت منجر به شکست زنجیره اصلی میشود. بنابراین، حضور اکسیژن عملاً مانع از اتصال عرضی (Cross-linking) شده و سطح پلیمر را ترد و شکننده میکند. این پدیده معمولاً «محدود به نفوذ» (Diffusion Limited) است؛ یعنی لایههای سطحی که در تماس با اکسیژن هستند به شدت اکسید و تخریب میشوند، در حالی که عمق قطعه (که اکسیژن به آن نرسیده) ممکن است شبکهای شود.
اثر دما و دمای انتقال شیشهای ($T_g$) بر تحرک رادیکالها
دما به عنوان موتور محرک مولکولی، نقش کلیدی در سینتیک رادیولیز ایفا میکند. رفتار رادیکالهای آزاد در دماهای پایینتر و بالاتر از «دمای انتقال شیشهای» ($T_g$) کاملاً متفاوت است.
در دماهای پایینتر از $T_g$ (ناحیه شیشهای)، زنجیرههای پلیمری “منجمد” هستند و تحرک بسیار کمی دارند. در این حالت، رادیکالهای تولید شده در قفسهای پلیمری به دام میافتند و نمیتوانند برای واکنش با یکدیگر جابجا شوند. این رادیکالهای به دام افتاده (Trapped Radicals) ممکن است تا مدتها پس از پایان تابش در ساختار باقی بمانند و بعدها با افزایش دما یا نفوذ اکسیژن فعال شوند (اثرات پس از تابش).
اما در دماهای بالاتر از $T_g$ (ناحیه لاستیکی)، زنجیرهها آزادی حرکت دارند. این تحرک پذیری باعث میشود رادیکالها راحتتر به هم رسیده و واکنشهای دوقطبی (مانند شبکهای شدن یا جدایش نامتناسب) با سرعت بیشتری رخ دهند. معمولاً افزایش دما حین تابشدهی، بازده شبکهای شدن را در پلیمرهایی مثل پلیاتیلن افزایش میدهد، زیرا شانس فرار رادیکالها از قفس اولیه بیشتر میشود.
تاثیر بلورینگی و نواحی آمورف بر بازده رادیولیز
بیشتر پلیمرهای صنعتی نیمهکریستالی هستند، یعنی ترکیبی از نواحی منظم (بلوری) و نامنظم (آمورف) دارند. نفوذپذیری گازها و تحرک رادیکالها در این دو ناحیه یکسان نیست. تجربه نشان میدهد که اکثر واکنشهای شیمیایی موثر در رادیولیز (چه اکسیداسیون و چه شبکهای شدن) در “فاز آمورف” رخ میدهند.
در نواحی بلوری، به دلیل فشردگی شدید زنجیرهها، رادیکالها اغلب بیحرکت مانده و در ساختار کریستال حبس میشوند. این نواحی کریستالی مانند “مخازن رادیکال” عمل میکنند. رادیکالهای حبس شده در کریستال، در اثر گذشت زمان به آرامی به سطح کریستال مهاجرت کرده و یا در صورت ذوب شدن پلیمر، ناگهان آزاد میشوند. این آزادسازی ناگهانی میتواند منجر به اکسیداسیون سریع پلیمر در مراحل پس از فرآورش شود. به همین دلیل، پلیمرهایی با درصد آمورف بالاتر، معمولاً پاسخ سریعتر و یکنواختتری به تابش میدهند.
اثر نرخ دوز (Dose Rate Effect) در آزمایشهای طولانیمدت
یکی از پیچیدهترین مفاهیم در پیشبینی عمر پلیمرها، تفاوت بین آزمایشهای سریع آزمایشگاهی و شرایط واقعی محیطی است. اگر یک مقدار ثابت انرژی (مثلاً ۱۰۰ کیلوگری) را با “نرخ دوز بالا” (در چند ثانیه) به پلیمر بدهیم، نتیجه متفاوت از زمانی است که همان مقدار انرژی را با “نرخ دوز پایین” (در طول چند سال) اعمال کنیم.
در نرخ دوز بالا، سرعت تولید رادیکالها بسیار بیشتر از سرعت نفوذ اکسیژن به داخل قطعه است. بنابراین، اکسیژن موجود در سطح سریعاً مصرف شده و لایههای داخلی دچار کمبود اکسیژن میشوند و تخریب اکسایشی رخ نمیدهد. اما در نرخ دوز پایین (مانند شرایط نیروگاههای هستهای یا فضایی)، اکسیژن زمان کافی دارد تا همگام با تولید رادیکالها به عمق قطعه نفوذ کند. این باعث میشود که تخریب در تمام حجم قطعه رخ دهد. به همین دلیل، آزمونهای شتابدهی شده با دوز بالا، اغلب عمر پلیمر را بیش از حد واقعی تخمین میزنند و پدیده رادیولیز اکسایشی همگن را نادیده میگیرند.
رادیولیز در حالت محلول آبی پلیمر (تفاوت با حالت جامد)
زمانی که پلیمر به صورت محلول (بهویژه در آب) تحت تابش قرار میگیرد، مکانیزم رادیولیز از «اثر مستقیم» به «اثر غیرمستقیم» تغییر ماهیت میدهد. در این حالت، این مولکولهای حلال (آب) هستند که بیشترین انرژی پرتو را جذب میکنند، زیرا غلظت آنها بسیار بیشتر از پلیمر است.
تابش به آب منجر به تولید گونههای بسیار فعال مانند «رادیکال هیدروکسیل» ($OH^\bullet$)، اتم هیدروژن ($H^\bullet$) و الکترونهای هیدراته ($e^-_{aq}$) میشود. این گونهها که تحرک بسیار بالایی در محیط مایع دارند، به زنجیرههای پلیمری حمله کرده و باعث انتقال واکنش میشوند.
$$H_2O \xrightarrow{Radiation} OH^\bullet + H^\bullet + e^-_{aq}$$
به دلیل تحرک بالای این واسطهها در فاز مایع، بازده واکنشها در محلول بسیار بالاتر از حالت جامد است. حتی دوزهای بسیار پایین پرتو در محلول آبی میتواند منجر به تغییرات ویسکوزیته شدید (تخریب یا ژل شدن) شود، در حالی که همان دوز در حالت جامد اثر ناچیزی دارد. این روش اساس تولید هیدروژلهای پزشکی استریلیزه است
رفتار رادیولیز در پلیاولفینها (PE, PP)
پلیاولفینها به عنوان گستردهترین خانواده پلیمری، آزمایشگاهی عالی برای درک اثر ساختار شیمیایی بر رادیولیز هستند. اگرچه پلیاتیلن (PE) و پلیپروپیلن (PP) هر دو هیدروکربنهای اشباع هستند و شباهت ظاهری زیادی دارند، اما پاسخ آنها به میدانهای تابشی کاملاً متضاد است. این تفاوت رفتار، اصلیترین معیار در انتخاب مواد برای کاربردهای هستهای و پزشکی محسوب میشود.
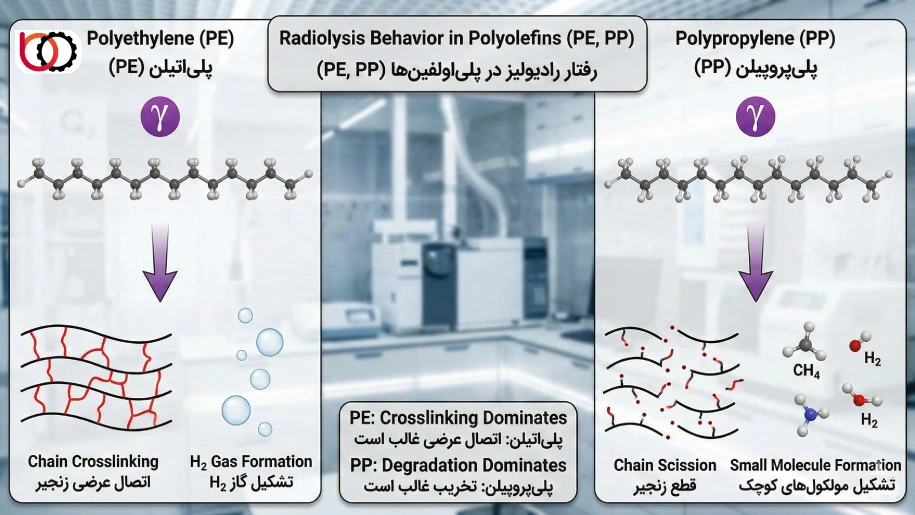
۱. پلیاتیلن (PE): الگوی شبکهای شدن
پلیاتیلن را نمونه ایدهآل برای فرآیندهای اصلاح پرتویی میدانند. ساختار تکرارشونده آن ($-CH_2-CH_2-$) ساده و فاقد گروههای جانبی مزاحم است. زمانی که انرژی پرتو جذب میشود، اصلیترین رویداد، کنده شدن اتمهای هیدروژن و ایجاد رادیکالهای ثانویه روی زنجیره است. این رادیکالها به دلیل نبود ممانعت فضایی، به راحتی به رادیکالهای زنجیره مجاور نزدیک شده و واکنش بازترکیب (Recombination) را انجام میدهند.
در پلیاتیلن، بازده کوانتومی اتصال عرضی ($G(X)$) همواره بر بازده قطع زنجیر ($G(S)$) غلبه دارد. نتیجه نهایی تابش، تبدیل ساختار خطی ترموپلاستیک به ساختاری سهبعدی و شبکهای است که در برابر حرارت جریان نمییابد (مانند لولههای PEX). البته در گریدهای سنگین (HDPE) به دلیل درصد بالای بلورینگی، بخشی از رادیکالها در نواحی کریستالی حبس شده و غیرفعال میمانند، اما رفتار غالب سیستم همچنان به سمت تقویت خواص مکانیکی و حرارتی است.
۲. پلیپروپیلن (PP): حساسیت شدید به تخریب
در سوی دیگر، پلیپروپیلن رفتاری کاملاً متفاوت از خود نشان میدهد. وجود گروه متیل ($-CH_3$) متصل به زنجیره اصلی، باعث ایجاد «کربن نوع سوم» (Tertiary Carbon) در هر واحد تکرارشونده میشود. رادیکالهای تشکیل شده روی این کربن، تمایل ترمودینامیکی بالایی به انجام واکنش «شکست بتا» دارند.
در رادیولیز پلیپروپیلن، پدیده قطع زنجیر مکانیزم مسلط است. انرژی پرتو به جای ایجاد اتصالات مفید، صرف شکستن اسکلت اصلی پلیمر میشود. این امر باعث افت سریع وزن مولکولی و کاهش شدید استحکام ضربه میگردد، به طوری که قطعات PP معمولی حتی در دوزهای پایین استریلیزاسیون (حدود ۲۵ کیلوگری) دچار تردی و پودر شدگی میشوند. علاوه بر این، محصولات جانبی اکسایشی در PP پایدارتر بوده و باعث زرد شدن قطعه میشوند. از این رو، استفاده از PP در محیطهای پرتویی نیازمند فرمولاسیونهای بسیار خاص با آنتیاکسیدانهای قوی است.
حساسیت پرتویی در پلیمرهای هالوژندار (PVC, PTFE)
در مهندسی پلیمر، جایگزینی اتمهای هیدروژن با هالوژنهای سنگین (مانند کلر و فلوئور)، معمولاً مقاومت شیمیایی و حرارتی ماده را افزایش میدهد. اما در دنیای رادیولیز، این قاعده اغلب معکوس عمل میکند. پلیمرهای هالوژندار به دلیل داشتن اتمهایی با چگالی الکترونی بالا، سطح مقطع جذب انرژی بزرگتری دارند و واکنشهای تخریبی شدیدی را تجربه میکنند که نه تنها خواص مکانیکی را از بین میبرد، بلکه میتواند منجر به تولید محصولات جانبی خورنده شود.

۱. پلیوینیل کلراید (PVC): پدیده رنگی شدن و آزادسازی اسید
رفتار رادیولیز در PVC تحت سلطه واکنشی به نام «هیدروکلریناسیونزدایی» (Dehydrochlorination) است. زمانی که پرتو به زنجیره PVC برخورد میکند، پیوند کربن-کلر ($C-Cl$) که ضعیفتر از پیوند کربن-کربن است، میشکند. رادیکال کلر جدا شده با جذب یک هیدروژن از کربن مجاور، مولکول اسید هیدروکلریک ($HCl$) را تشکیل داده و از سیستم خارج میشود.
خروج $HCl$ باعث ایجاد یک پیوند دوگانه در زنجیره میشود. نکته بحرانی اینجاست که وجود این پیوند دوگانه، پیوندهای مجاور را ناپایدار کرده و باعث خروج زنجیرهای مولکولهای $HCl$ بعدی میشود (اثر زیپ). این فرآیند منجر به تشکیل توالیهای طولانی از پیوندهای دوگانه مزدوج (Polyenes) میگردد که عامل اصلی تغییر رنگ شدید PVC از شفاف به زرد، قهوهای و در نهایت سیاه است. این تغییر رنگ حتی در دوزهای پایین نیز مشاهده میشود و استفاده از PVC در تجهیزات پزشکی استریل شده با پرتو را محدود میکند.
۲. پلیتترافلوئورواتیلن (PTFE): پارادوکس مقاومت
تفلون یا PTFE یکی از عجیبترین رفتارها را در علم مواد دارد. اگرچه این پلیمر در برابر قویترین اسیدها و حلالها مقاوم است، اما در برابر تجزیه پرتویی یکی از ضعیفترین پلیمرهای شناخته شده محسوب میشود. در ساختار PTFE، اتمهای فلوئور با حجم زیاد و دافعه الکترواستاتیک بالا، اطراف زنجیره کربنی را احاطه کردهاند.
زمانی که انرژی پرتو پیوند کربن-کربن اسکلت اصلی را میشکند، دو رادیکال انتهایی تشکیل میشوند. برخلاف پلیاتیلن، در اینجا به دلیل ممانعت فضایی شدید اتمهای فلوئور و عدم امکان انتقال هیدروژن (چون هیدروژنی وجود ندارد)، رادیکالها نمیتوانند دوباره به هم متصل شوند (بازترکیب رخ نمیدهد). در نتیجه، واکنشهای قطع زنجیر با شدت تمام پیش میروند. تخریب PTFE چنان سریع است که حتی دوزهای بسیار پایین (کمتر از ۵ کیلوگری) باعث کاهش شدید وزن مولکولی و تبدیل شدن قطعه مستحکم به پودری مومیشکل میشود. در صنعت، از این خاصیت تخریبپذیری به صورت کنترل شده برای تولید میکروپودرهای تفلون (جهت استفاده در روانکارها) بهرهبرداری میشود.
پایداری پرتویی در پلیمرهای آروماتیک (PS, PET)
در طیف وسیع مواد پلیمری، پلیمرهای حاوی حلقههای آروماتیک (بنزن) رفتاری متمایز از خود نشان میدهند. این مواد به عنوان ساختارهای مقاوم در برابر پرتو شناخته میشوند. برخلاف پلیاولفینها یا پلیمرهای هالوژندار که به سرعت وارد واکنشهای شیمیایی میشوند، پلیمرهای آروماتیک توانایی بالایی در جذب و دفع بیخطر انرژی تابشی دارند، بدون اینکه دچار تغییرات ساختاری عمده شوند. این ویژگی ناشی از ساختار الکترونی خاص حلقه بنزن است.
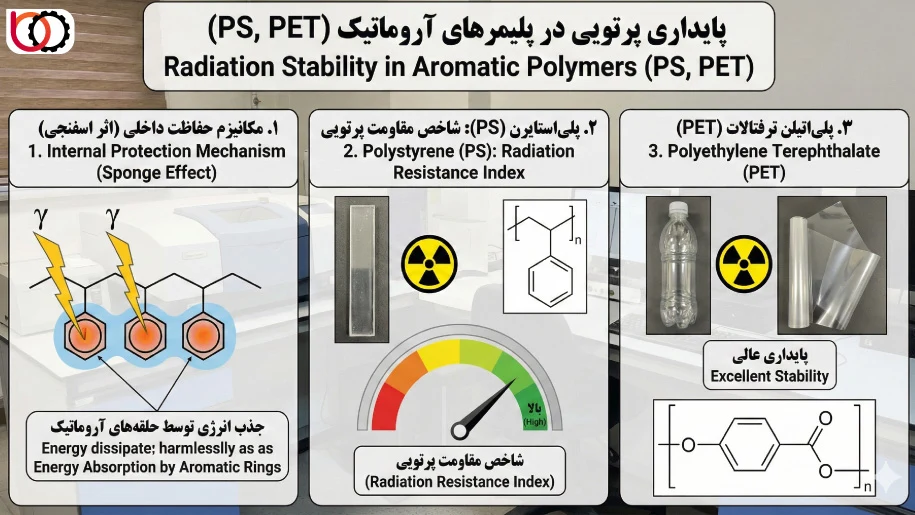
۱. مکانیزم حفاظت داخلی (اثر اسفنجی)
دلیل اصلی پایداری این مواد، وجود الکترونهای $\pi$ غیرمستقر در حلقه آروماتیک است. این سیستم الکترونی دارای ترازهای انرژی برانگیخته متعددی است که فاصله انرژی کمی با هم دارند. زمانی که پرتو به پلیمر برخورد میکند، انرژی جذب شده به سرعت به حلقههای آروماتیک منتقل میشود. حلقه بنزن مانند یک «اسفنج انرژی» (Energy Sink) عمل کرده و این انرژی را جذب میکند. سپس به جای اینکه پیوند شیمیایی بشکند، انرژی جذب شده به صورت نور (فلورسانس) یا گرما به محیط بازگردانده میشود. این فرآیند اتلاف فیزیکی انرژی، باعث میشود بازده واکنشهای شیمیایی (مقادیر $G$) در این پلیمرها بسیار پایین باشد.
۲. پلیاستایرن (PS): شاخص مقاومت پرتویی
پلیاستایرن یکی از پایدارترین پلیمرهای متداول در برابر رادیولیز است. وجود گروه فنیل آویزان در هر واحد تکرارشونده، محافظتی موثر برای زنجیره اصلی فراهم میکند. مطالعات نشان میدهند که برای ایجاد تغییرات قابل اندازهگیری در خواص مکانیکی PS، به دوزهای تابش بسیار بالایی (بیش از ۱۰ مگاگری) نیاز است که صدها برابر دوز استریلیزاسیون معمولی است. به همین دلیل، قطعات ساخته شده از پلیاستایرن (مانند ظروف پتری دیش آزمایشگاهی) بدون هیچگونه تغییر رنگ یا شکنندگی، فرآیندهای تابشدهی را تحمل میکنند.
۳. پلیاتیلن ترفتالات (PET)
در PET، حلقههای آروماتیک درون اسکلت اصلی پلیمر قرار دارند. اگرچه وجود گروههای استری ($-COO-$) نقاطی مستعد برای شکست هستند، اما حضور حلقه بنزن در مجاورت آنها، پایداری کلی زنجیره را حفظ میکند. رادیولیز در PET معمولاً منجر به تغییرات جزئی در وزن مولکولی میشود و خواص کششی و نفوذپذیری آن تا دوزهای بالا ثابت میماند. این ویژگی باعث شده است که PET گزینهای مطلوب برای بستهبندیهای پزشکی و غذایی باشد که نیاز به استریلیزاسیون با پرتو دارند.
رادیولیز در پلیمرهای زیستتخریبپذیر (PLA, Starch)
با گسترش استفاده از پلیمرهای زیستتخریبپذیر در کاربردهای پزشکی (مانند نخهای بخیه و ایمپلنتها) و بستهبندی، شناخت رفتار آنها در برابر فرآیندهای استریلیزاسیون پرتویی اهمیت ویژهای یافته است. این پلیمرها که اغلب دارای ساختارهای هیدرولیزپذیر هستند، در مواجهه با رادیولیز حساسیتی بالا و واکنشی سریع از خود نشان میدهند. در اینجا، هدف مهندسی معمولاً حفظ تعادل میان استریلیته و عدم تخریب زودرس خواص مکانیکی است.
۱. پلیلاکتیک اسید (PLA): تسلط مکانیزم شکست
پلیلاکتیک اسید به عنوان پرمصرفترین پلیمر زیستی مصنوعی، دارای پیوندهای استری ($-COO-$) در زنجیره اصلی خود است. در فرآیند رادیولیز، این پیوندهای استری نقاط ضعف اصلی محسوب میشوند. مطالعات نشان میدهند که در PLA، پدیده قطع زنجیر (Chain Scission) بر شبکهای شدن غلبه دارد. انرژی پرتو باعث شکستن پیوند $C-O$ در گروه استری شده و منجر به کاهش سریع وزن مولکولی متوسط ($M_w$) میشود.
این کاهش وزن مولکولی، دو پیامد مهم دارد: اول، افزایش شکنندگی و کاهش استحکام کششی قطعه؛ و دوم، افزایش نرخ زیستتخریبپذیری. زنجیرههای کوتاهتر سریعتر هیدرولیز میشوند. بنابراین، مهندسین پزشکی از دوزهای کنترلشده تابش استفاده میکنند تا زمان جذب ایمپلنتهای PLA در بدن را تنظیم کنند. اگر دوز تابش بالا باشد، ایمپلنت قبل از بهبود بافت بیمار، ساختار خود را از دست میدهد.
۲. نشاسته (Starch): تخریب ساختار پلیساکاریدی
نشاسته به عنوان یک پلیمر طبیعی، از واحدهای گلوکز که با پیوندهای گلیکوزیدی ($C-O-C$) به هم متصل شدهاند، تشکیل شده است. این پیوندهای اتری در برابر تجزیه پرتویی بسیار آسیبپذیر هستند. تابشدهی به نشاسته، حتی در دوزهای پایین، باعث شکست گسترده پیوندهای گلیکوزیدی و فروپاشی ساختار ماکرومولکولی میشود.
نتیجه فیزیکی این فرآیند، کاهش شدید ویسکوزیته و حلالیت بیشتر در آب است. اگرچه این تخریب برای کاربردهای ساختاری مضر است، اما در صنایع شیمیایی از آن بهرهبرداری میشود. رادیکالهای ایجاد شده روی بدنه نشاسته در حین تابش، مکانهایی عالی برای انجام واکنشهای “پیوندزنی” (Grafting) هستند. با افزودن مونومرهای وینیل به نشاسته تحت تابش، کوپلیمرهایی تولید میشوند که خواص جذب آب فوقالعادهای دارند (سوپرجاذبها) و در محصولات بهداشتی استفاده میشوند.
اثر پرتو بر سلولز و پلیمرهای طبیعی
سلولز به عنوان فراوانترین پلیمر طبیعی، ساختاری متشکل از واحدهای گلوکز دارد که با پیوندهای $\beta(1\to4)$ گلیکوزیدی به یکدیگر متصل شدهاند. برخلاف پلیاولفینها که امکان شبکهای شدن دارند، پلیمرهای طبیعی و بهویژه پلیساکاریدها (مانند سلولز، کیتوسان و آلژینات) تحت تابش پرتوهای یونساز، تقریباً به صورت انحصاری دچار تخریب زنجیره (Degradation) میشوند. در این مواد، انرژی پرتو بر نقاط اتصال ضعیف بین واحدها متمرکز شده و ساختار ماکرومولکولی را میشکند.
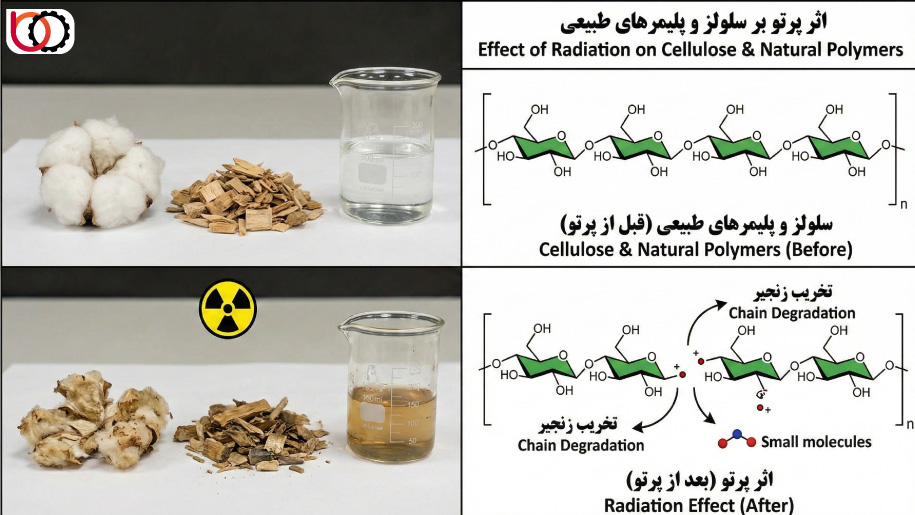
۱. مکانیزم شکست پیوند گلیکوزیدی
ضعیفترین نقطه در زنجیره سلولز، پیوند اتری $C-O-C$ بین حلقههای گلوکز است. زمانی که پرتو به ساختار برخورد میکند، اتمهای هیدروژن متصل به کربنهای شماره ۱، ۴ یا ۵ در حلقه گلوکز جدا میشوند (انتزاع هیدروژن). رادیکالهای ایجاد شده ناپایدار بوده و منجر به شکستن پیوند گلیکوزیدی میشوند. این پدیده باعث کاهش سریع «درجه پلیمریزاسیون» (DP) میشود. رابطه بین دوز تابش ($D$) و کاهش وزن مولکولی در سلولز از معادله چارلزبی پیروی میکند:
$$\frac{1}{DP_D} – \frac{1}{DP_0} = k \cdot D$$
در این رابطه، $DP_D$ درجه پلیمریزاسیون پس از تابش و $DP_0$ مقدار اولیه آن است. شیب خط ($k$) نشاندهنده حساسیت ذاتی پلیمر به تخریب است.
۲. تغییرات در نواحی کریستالی و آمورف
سلولز دارای ساختاری بسیار منظم و کریستالی (به دلیل پیوندهای هیدروژنی قوی بین زنجیرهها) است. اگرچه واکنشهای شیمیایی اولیه در هر دو ناحیه کریستالی و آمورف رخ میدهند، اما نفوذ اکسیژن به نواحی کریستالی محدود است. رادیکالهای آزاد تشکیل شده در نواحی کریستالی (Trapped Radicals) بسیار پایدار هستند و نمیتوانند به راحتی با اکسیژن واکنش دهند یا با سایر رادیکالها بازترکیب شوند. مشاهده میشود که این رادیکالها تا مدتها پس از فرآیند تابشدهی در ساختار باقی میمانند و عامل اصلی «تخریب تاخیری» (Post-irradiation degradation) در کاغذ و منسوجات پنبهای هستند.
۳.کاربردهای صنعتی تخریب سلولز
اگرچه کاهش استحکام مکانیکی معمولاً نامطلوب است، اما در صنایع ویسکوز و استات سلولز، از رادیولیز به عنوان یک ابزار فرآیندی دقیق استفاده میشود. تابشدهی به پالپ (خمیر کاغذ) باعث کاهش ویسکوزیته و افزایش واکنشپذیری شیمیایی آن میشود. این امر نیاز به استفاده از مواد شیمیایی مخرب زیستمحیطی و زمان طولانی “رسیدن” (Aging) در فرآیند تولید ویسکوز را حذف میکند. همچنین در تولید بیواتانول، پیشتیمار سلولز با پرتو الکترون، ساختار کریستالی را بهم ریخته و دسترسی آنزیمها برای هیدرولیز قندها را تسهیل میکند.
۴. چالشهای استریلیزاسیون محصولات سلولزی
در کاربردهای پزشکی (مانند گاز استریل و لباسهای بیمارستانی)، سلولز باید دوز استریلیزاسیون (۲۵ کیلوگری) را تحمل کند. مشکل اصلی در اینجا، زرد شدن (Yellowing) و ترد شدن الیاف است. تشکیل گروههای کربونیل ($C=O$) و کربوکسیل ($COOH$) در اثر اکسیداسیون پرتویی، باعث تغییر رنگ پنبه میشود. برای مقابله با این پدیده، کنترل دقیق رطوبت نمونه و استفاده از نرخ دوز بالا (برای کاهش زمان تماس با اکسیژن) ضروری است.
این بخش به بررسی رفتار گروه مهمی از پلاستیکهای مهندسی میپردازد که در صنایع نساجی، خودرو و قطعات الکتریکی کاربرد وسیع دارند و رفتار آنها تحت تابش به شدت به شرایط محیطی وابسته است:
تخریب پرتویی در پلیآمیدها و نایلونها
پلیآمیدها (مانند نایلون ۶ و نایلون ۶۶) به دلیل داشتن پیوندهای هیدروژنی بینزنجیری قوی و ساختار کریستالی، خواص مکانیکی و حرارتی ممتازی دارند. در مواجهه با فرآیند رادیولیز، رفتار این پلیمرها حاصل رقابت تنگاتنگ بین دو پدیده قطع زنجیر و شبکهای شدن است. جهت پیشرفت واکنش در این مواد، بیش از هر پلیمر دیگری به حضور یا عدم حضور اکسیژن بستگی دارد.
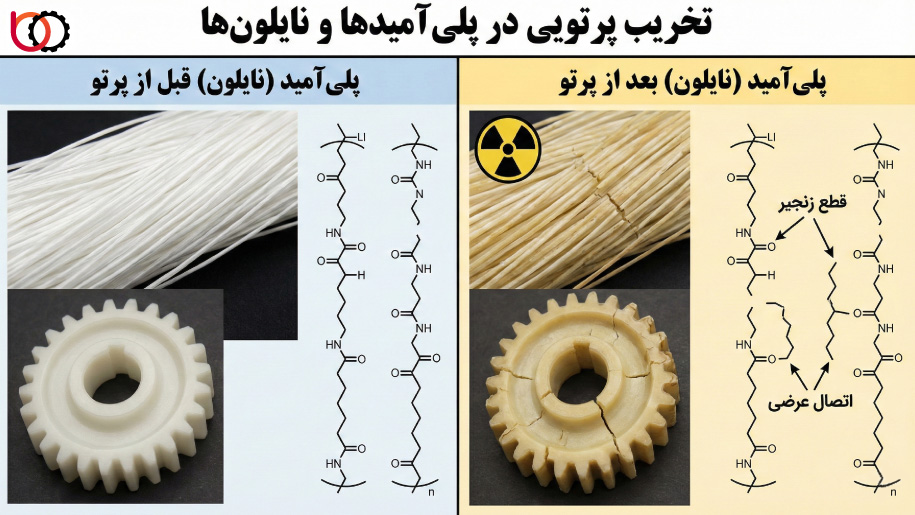
۱. محل تشکیل رادیکال اولیه
حمله پرتو به زنجیره پلیآمید، گزینشی عمل میکند. ضعیفترین پیوند $C-H$ در ساختار نایلون، مربوط به اتم کربنی است که در مجاورت گروه نیتروژن (گروه آمینی) قرار دارد. اتم نیتروژن با خاصیت الکترونکشندگی خود، پیوند $C-H$ همسایه را تضعیف میکند. بنابراین، مکانیسم اولیه شامل جدا شدن هیدروژن از کربن آلفا نسبت به نیتروژن است:
$$-CO-NH-CH_2- \xrightarrow{Radiation} -CO-NH-\dot{C}H- + H^\bullet$$
رادیکال تشکیل شده ($-\dot{C}H-$) مرکز اصلی تمام واکنشهای بعدی محسوب میشود.
۲. دوگانگی رفتار در خلأ و هوا
اگر تابشدهی در محیط خنثی یا خلأ انجام شود، رادیکالهای پلیمری مجاور با یکدیگر ترکیب شده و اتصالات عرضی تشکیل میدهند. این پدیده باعث افزایش وزن مولکولی و بهبود خواص سایشی نایلون میشود.
اما در شرایط اتمسفریک (حضور هوا)، داستان کاملاً متفاوت است. رادیکالهای کربن آلفا به شدت با اکسیژن واکنش داده و تشکیل پرواکسید میدهند. تجزیه این پرواکسیدها منجر به شکستن پیوند پپتیدی ($C-N$) در زنجیره اصلی میشود:
$$-CO-NH- \xrightarrow{Oxidation} \text{Chain Scission} + \text{Carbonyl Groups}$$
به همین دلیل، الیاف و قطعات نایلونی که در هوا پرتو میبینند، دچار افت شدید استحکام کششی شده و سطح آنها به سرعت پودر میشود.
۳. زرد شدن (Yellowing) و تغییرات ظاهری
یکی از مشکلات بارز در استریلیزاسیون محصولات نایلونی، تغییر رنگ سریع آنهاست. تشکیل گروههای کربونیل مزدوج و ایمیدهای حلقوی در اثر اکسیداسیون، باعث میشود نایلون شفاف یا سفید، به رنگ زرد کدر تغییر یابد. این تغییر رنگ حتی با دوزهای پایین پرتو نیز رخ میدهد و اغلب به عنوان نشانه ظاهری تخریب در نظر گرفته میشود.
۴. اثر رطوبت بر رادیولیز نایلون
نایلونها پلیمرهایی جاذب رطوبت (Hygroscopic) هستند. مولکولهای آب جذب شده در ساختار نایلون، در فرآیند رادیولیز نقش واسطه را بازی میکنند. آب تحت تابش به رادیکالهای هیدروکسیل ($OH^\bullet$) تجزیه میشود که این رادیکالها حمله شیمیایی به زنجیره پلیمر را تشدید میکنند. بنابراین، نایلون مرطوب نسبت به نایلون خشک، حساسیت بیشتری به تخریب پرتویی دارد و افت خواص در آن سریعتر اتفاق میافتد.
رفتار رزینهای اپوکسی و گرماسختها در برابر پرتو
رزینهای گرماسخت (Thermosets) مانند اپوکسیها، فنولیکها و پلیاسترهای غیراشباع، برخلاف ترموپلاستیکها، دارای ساختاری سهبعدی و تماماً شبکهای هستند. این ساختار صلب باعث میشود که رفتار آنها در برابر رادیولیز، نه به صورت تغییر فرم یا ذوب شدن، بلکه به صورت تردی فزاینده و ایجاد تنشهای داخلی بروز کند. به طور کلی، رزینهای اپوکسی پخت شده (Cured Epoxies) مقاومت پرتویی بسیار بالایی دارند و تغییرات خواص مکانیکی در آنها تا دوزهای بسیار بالا (حدود ۱۰ مگاگری) محسوس نیست.

۱. نقش ساختار آروماتیک در پایداری
بیشتر رزینهای اپوکسی صنعتی بر پایه «بیسفنول آ» (Bisphenol A) هستند. حضور دو حلقه بنزن در هر واحد تکرارشونده این رزین، خاصیت حفاظتی (Energy Dissipation) فوقالعادهای ایجاد میکند. انرژی پرتو توسط حلقههای آروماتیک جذب و بدون شکستن پیوندهای اصلی، دفع میشود. با این حال، نقاط ضعف این رزینها، پیوندهای آلیفاتیک در عامل پخت (Hardener) و اتصالات اتری است.
۲. مشکل محبوس شدن گازها (Gas Trapping):
در ترموپلاستیکها، گازهای تولید شده ($H_2, CH_4$) میتوانند با نفوذ از بین زنجیرهها خارج شوند. اما در گرماسختها، تراکم بالای شبکه اجازه خروج گاز را نمیدهد. تجمع مولکولهای گاز در فضای بسته شبکه، باعث افزایش فشار داخلی میشود. وقتی این فشار از استحکام کششی موضعی رزین فراتر رود، ترکهای ریز داخلی (Micro-cracking) یا پدیده Crazing رخ میدهد. این ترکها مسیر نفوذ اکسیژن را باز کرده و تخریب را تسریع میکنند.
۳. پخت تابشی رزینهای اپوکسی (Radiation Curing)
علاوه بر بحث تخریب، یکی از کاربردهای پیشرفته صنعتی، استفاده از پرتو الکترون (EB) برای پخت رزینهای اپوکسی خام است. برخلاف پخت حرارتی که زمانبر است، پخت پرتویی با استفاده از «آغازگرهای کاتیونی» (Cationic Initiators) انجام میشود. پرتو باعث شکستن نمکهای اونیوم موجود در مخلوط شده و اسید لوئیس تولید میکند که کاتالیزور پلیمریزاسیون اپوکسی است.
این روش در ساخت کامپوزیتهای پیشرفته هوافضا (مانند فیبر کربن-اپوکسی) استفاده میشود. مزیت بزرگ آن، انجام فرآیند در دمای محیط است که از ایجاد تنشهای حرارتی پسماند در قطعه جلوگیری میکند و امکان تولید قطعاتی با پایداری ابعادی بسیار دقیق را فراهم میآورد.
رادیولیز در لاستیکهای سیلیکونی (PDMS)
لاستیکهای سیلیکونی یا پلیدیمتیلسیلوکسان (PDMS)، دارای اسکلتی متشکل از پیوندهای متناوب سیلسیم-اکسیژن ($-Si-O-$) هستند که انرژی پیوندی بالاتری نسبت به پیوند کربن-کربن دارد. این ویژگی باعث میشود که زنجیره اصلی در برابر شکست حرارتی و پرتویی مقاوم باشد. در فرآیند رادیولیز، تمرکز واکنشها نه بر روی اسکلت اصلی، بلکه بر روی گروههای جانبی متیل ($-CH_3$) است.

۱. غلبه شبکهای شدن بر تخریب
رفتار غالب سیلیکونها در برابر پرتوهای یونساز، شبکهای شدن (Cross-linking) است. مقدار $G(X)$ در این مواد به مراتب بزرگتر از $G(S)$ است. مکانیزم اصلی شامل جدا شدن اتم هیدروژن از گروه متیل و تشکیل رادیکال متیلن روی زنجیره است:
$$\equiv Si-CH_3 \xrightarrow{Radiation} \equiv Si-\dot{C}H_2 + H^\bullet$$
سپس دو رادیکال متیلن مجاور با هم ترکیب شده و یک پل اتیلنی ($-CH_2-CH_2-$) بین دو زنجیره سیلوکسان ایجاد میکنند. همچنین امکان تشکیل پلهای متیلنی ($-CH_2-$) از طریق حمله رادیکال به گروه متیل همسایه نیز وجود دارد.
۲. تغییرات خواص فیزیکی
نتیجه مستقیم این اتصالات عرضی اضافی، افزایش مدول الاستیک و سختی لاستیک است. با افزایش دوز تابش، سیلیکون نرم و انعطافپذیر به مرور سفتتر شده و قابلیت کشسانی (Elongation at Break) آن کاهش مییابد. اگر دوز تابش بسیار بالا باشد (بیش از چند صد کیلوگری)، لاستیک سیلیکونی تبدیل به مادهای شکننده و شیشه-مانند میشود.
۳. نقش فیلرها و افزودنیها
لاستیکهای سیلیکونی صنعتی معمولاً حاوی مقادیر زیادی فیلر تقویتکننده مانند سیلیکا ($SiO_2$) هستند. مشاهده میشود که انتقال انرژی در فصلمشترک پلیمر و ذرات فیلر، میتواند بازده رادیولیز را تغییر دهد. همچنین، وارد کردن گروههای فنیل (حلقه بنزن) در ساختار سیلیکون (پلیمتیلفنیلسیلوکسان)، مقاومت پرتویی را به شدت افزایش میدهد. همانند پلیاستایرن، گروههای فنیل در اینجا نیز انرژی را جذب و مستهلک میکنند و مانع از سفت شدن سریع لاستیک در محیطهای هستهای میشوند.
۴. گازهای تولیدی
محصولات گازی حاصل از رادیولیز سیلیکون عمدتاً هیدروژن، متان و اتان هستند. خروج این گازها از درون قطعات ضخیم سیلیکونی دشوار است و ممکن است باعث ایجاد تخلخل یا حبابهای ریز در ساختار داخلی قطعه شود که خواص دیالکتریک (عایق الکتریکی) آن را تضعیف میکند.
کاربردهای نوین رادیولیز در صنعت
امروزه رادیولیز دیگر تنها یک پدیده جانبی ناخواسته در صنعت هستهای نیست؛ بلکه به عنوان یک فناوری فرآوری پیشرفته (Radiation Processing) شناخته میشود. با کنترل دقیق دوز، نرخ دوز و محیط واکنش، مهندسین پلیمر از انرژی پرتو برای ایجاد ساختارهای مولکولی پیچیدهای استفاده میکنند که تولید آنها با روشهای شیمیایی متداول یا غیرممکن است و یا هزینه بسیار بالایی دارد. در ادامه مهمترین کاربردهای صنعتی این فناوری بررسی میشود.

تولید هیدروژلهای پزشکی با رادیولیز
یکی از “پاکترین” روشهای تولید هیدروژل برای پانسمانهای سوختگی و سیستمهای دارورسانی، استفاده از پرتو الکترون یا گاما است. در روشهای شیمیایی معمول، برای ایجاد شبکه سهبعدی نیاز به افزودن عوامل شبکهایکننده (Cross-linkers) سمی است که حذف کامل آنها از محصول نهایی دشوار است. اما در روش پرتویی، رادیولیز آب نقش اصلی را ایفا میکند.
زمانی که محلول آبی یک پلیمر زیستسازگار (مانند پلیوینیل پیرولیدون یا PVP) تحت تابش قرار میگیرد، رادیکالهای هیدروکسیل ($OH^\bullet$) تولید شده از آب، به زنجیرههای پلیمر حمله کرده و ماکرورادیکالها را میسازند. بازترکیب این ماکرورادیکالها منجر به تشکیل شبکه ژلی میشود. مزیت بزرگ این روش، انجام همزمان فرآیند «شبکهای شدن» و «استریلیزاسیون» در یک مرحله است. محصول نهایی فاقد هرگونه ماده شیمیایی سمی بوده و مستقیماً قابل استفاده در بدن انسان است.
پیوند زنی پرتویی (Grafting) برای اصلاح سطح
تکنیک «پیوند زنی» (Grafting) راهکاری هوشمندانه برای ترکیب خواص دو پلیمر متفاوت است. در این روش، از رادیولیز برای ایجاد رادیکالهای فعال تنها بر روی سطح یک پلیمر پایه (مثلاً فیلم پلیاتیلن) استفاده میشود. سپس این سطح فعال در معرض مونومر دیگری (مثلاً اکریلیک اسید) قرار میگیرد. رادیکالهای سطحی آغازگر پلیمریزاسیون مونومر دوم میشوند و شاخههای جدیدی روی تنه اصلی رشد میکنند.
این تکنیک کاربرد وسیعی در اصلاح غشاها و فیلترها دارد. برای مثال، با پیوند زدن گروههای آبدوست به سطح پلیمرهای آبگریز، غشاهایی برای تصفیه آب یا جداکننده باتریهای لیتیومی تولید میشود که ترشوندگی و عبوردهی یونی بسیار بالایی دارند، در حالی که استحکام مکانیکی آنها توسط پلیمر پایه تامین میشود.
کاربرد رادیولیز در بازیافت پسماندهای پلاستیکی
مدیریت پسماند پلیمرهایی که قابلیت ذوب مجدد ندارند (مانند لاستیکها و تفلون) یا وزن مولکولی بسیار بالایی دارند، یک چالش زیستمحیطی است. رادیولیز تخریبی در اینجا به عنوان یک راه حل بازیافت شیمیایی عمل میکند.
- بازیافت PTFE: ضایعات تفلون با دوزهای بالا پرتو میبینند تا زنجیرههای آنها شکسته شود (Scission). محصول حاصل، میکروپودرهایی با وزن مولکولی پایین است که به عنوان افزودنی روانکننده در جوهرها و روغنهای صنعتی کاربرد دارد.
- بازیافت لاستیک تایر: استفاده از پرتو الکترون برای شکستن انتخابی پیوندهای گوگردی (Devulcanization) در لاستیک فرسوده، امکان استفاده مجدد از آن را در آمیزههای لاستیکی جدید فراهم میکند.
- سلولز و زیستتوده: تابشدهی به پسماندهای کشاورزی باعث کاهش درجه پلیمریزاسیون سلولز شده و راندمان تبدیل آن به بیواتانول یا بیوگاز را به طرز چشمگیری افزایش میدهد.
لیتوگرافی با پرتو الکترونی در صنایع الکترونیک
دقیقترین کاربرد رادیولیز در ابعاد نانومتری، در صنعت تولید تراشههای الکترونیکی (Semiconductors) دیده میشود. در لیتوگرافی پرتو الکترونی (EBL)، یک لایه نازک پلیمری (Resist) روی ویفر سیلیکونی قرار میگیرد و توسط یک پرتو الکترونی متمرکز روبش میشود.
رفتار پلیمر تعیینکننده نوع لیتوگرافی است:
- رزیست مثبت (Positive Resist): پلیمرهایی مانند PMMA که تحت تابش دچار قطع زنجیر میشوند. نواحی تابش دیده محلول شده و شسته میشوند و طرح حفرهای ایجاد میکنند.
- رزیست منفی (Negative Resist): پلیمرهایی که تحت تابش شبکهای میشوند. نواحی تابش دیده نامحلول شده و باقی میمانند.این تکنیک امکان ایجاد الگوهای مداری با دقت زیر ۱۰ نانومتر را فراهم میکند که برای پردازندههای نسل جدید حیاتی است.
شبیهسازی تخریب فضایی در پلیمرهای ماهوارهای
پلیمرهای مورد استفاده در بدنه ماهوارهها و ایستگاههای فضایی (مانند پوششهای حرارتی Kapton یا عایقهای الکتریکی) در معرض تابش مداوم پروتونها و الکترونهای کمربند وان آلن هستند. رادیولیز در شرایط خلأ فضا و نوسانات دمایی شدید، رفتار متفاوتی دارد.
در آزمایشگاههای زمینی، از شتابدهندهها برای بمباران نمونههای پلیمری و شبیهسازی عمر ۲۰ ساله ماهواره در چند هفته استفاده میشود. بررسیها نشان میدهد که در خلأ، به دلیل نبود اکسیژن، واکنشهای قطع زنجیر و شبکهای شدن غالب هستند، اما عدم دفع گرما در خلأ میتواند منجر به افزایش دمای موضعی و تخریب حرارتی همزمان شود. این آزمونها برای تضمین عملکرد طولانیمدت قطعات پلیمری در مدار زمین (LEO/GEO) ضروری هستند.
روشهای پایدارسازی پلیمر در برابر پرتو
در بسیاری از کاربردهای صنعتی، استفاده از پلیمرهای ذاتاً مقاوم (مانند پلیاستایرن) به دلایل اقتصادی یا خواص مکانیکی مقدور نیست. بنابراین، مهندسین برای محافظت از پلیمرهای حساس (مانند PP یا PTFE) در برابر دوزهای بالای تابش، از استراتژی «پایدارسازی شیمیایی» استفاده میکنند. این حفاظت توسط افزودنیهای خاصی انجام میشود که در صنعت با نام عمومی «آنتیراد» (Antirad) شناخته میشوند. عملکرد این مواد بر اساس مداخله در یکی از مراحل سهگانه زمانی رادیولیز (فیزیکی یا شیمیایی) استوار است تا از پیشرفت واکنشهای زنجیرهای تخریب جلوگیری شود.
۱. گیراندازهای رادیکال (Radical Scavengers)
رایجترین مکانیزم عمل آنتیرادها، خنثیسازی رادیکالهای پلیمری فعال ($P^\bullet$) است. این ترکیبات معمولاً دارای هیدروژنهای لبیلی (Labile) هستند که به راحتی جدا میشوند. زمانی که رادیکال روی زنجیره پلیمر تشکیل میشود، قبل از اینکه فرصت قطع زنجیر یا حمله به اکسیژن را داشته باشد، با مولکول آنتیراد ($AH$) واکنش میدهد:
$$P^\bullet + AH \longrightarrow PH + A^\bullet$$
در این واکنش، رادیکال پلیمر با گرفتن هیدروژن “ترمیم” میشود ($PH$) و رادیکال جدیدی روی افزودنی ($A^\bullet$) شکل میگیرد. شرط کارایی آنتیراد این است که رادیکال $A^\bullet$ باید بسیار پایدار و غیرفعال باشد (معمولاً از طریق رزونانس حلقههای آروماتیک) تا واکنش زنجیرهای در همین نقطه متوقف شود. آمینهای آروماتیک ثانویه و فنولهای ممانعتشده (Hindered Phenols) از مهمترین مواد این گروه هستند.
۲. عوامل انتقال انرژی (Energy Transfer Agents)
این دسته از پایدارکنندهها در مرحله فیزیکی و قبل از شکستن پیوند عمل میکنند. این مولکولها دارای ترازهای انرژی برانگیخته پایینتری نسبت به پلیمر پایه هستند. زمانی که پلیمر انرژی پرتو را جذب کرده و برانگیخته میشود ($P^*$)، قبل از تفکیک پیوند، انرژی خود را به مولکول پایدارکننده ($A$) منتقل میکند:
$$P^* + A \longrightarrow P + A^*$$
سپس مولکول افزودنی برانگیخته ($A^*$)، انرژی دریافتی را به صورت گرما یا فلورسانس دفع میکند. ترکیبات آروماتیک چندحلقهای (مانند نفتالین و آنتراسن) یا مولکولهای دارای پیوندهای مزدوج طولانی، به عنوان “چاه انرژی” (Energy Sink) عمل کرده و شدت تخریب را به طور قابل توجهی کاهش میدهند. مشاهده میشود که افزودن تنها ۱ تا ۵ درصد از این مواد، میتواند مقاومت پرتویی را چندین برابر افزایش دهد.
۳. تجزیهکنندگان پراکسید (Peroxide Decomposers)
در شرایطی که تابشدهی در حضور هوا انجام میشود (یا اکسیداسیون پس از تابش مد نظر است)، صرفاً جمع کردن رادیکالها کافی نیست. باید از تجزیه هیدروپراکسیدهای تشکیل شده ($ROOH$) به رادیکالهای فعال جلوگیری کرد. ترکیبات آلی فسفیت (Phosphites) و تیواسترها (Thioesters) با کاهش دادن هیدروپراکسیدها به الکلهای پایدار (بدون تولید رادیکال)، چرخه اکسیداسیون خودشتابدهنده را قطع میکنند.
استفاده ترکیبی (Synergistic) از این افزودنیها در فرمولاسیون قطعات پزشکی و کابلهای هستهای، امری ضروری است تا اطمینان حاصل شود که خواص مکانیکی قطعه در طول عمر کاری حفظ میگردد.
افزودنیهای محافظ پرتویی (Antirads)
در صنعت فرمولاسیون پلیمر، به مجموعه ترکیباتی که به منظور کاهش اثرات مخرب پرتوهای یونساز به آمیزه پلیمری افزوده میشوند، اصطلاحاً «آنتیراد» (Antirad) گفته میشود. این مواد نقش «قربانی» را در سیستم ایفا میکنند؛ بدین معنا که با داشتن پتانسیل یونیزاسیون پایینتر یا تمایل بیشتر به جذب رادیکال نسبت به پلیمر پایه، خود را سپر بلا کرده و تخریب میشوند تا زنجیره پلیمری سالم بماند. انتخاب نوع آنتیراد به جنس پلیمر، دوز تابش و کاربرد نهایی قطعه وابسته است.

۱. آنتیاکسیدانها به عنوان آنتیراد
بسیاری از آنتیاکسیدانهای متداول حرارتی، رفتار آنتیرادی نیز از خود نشان میدهند، اما معمولاً باید با غلظتهای بالاتر (۰.۵ تا ۲ درصد وزنی) استفاده شوند.
- آمینهای آروماتیک: (مانند فنیل-بتا-نفتیلآمین) قویترین محافظها برای لاستیکها (مثل لاستیک استایرن-بوتادین SBR) هستند. این مواد به دلیل داشتن نیتروژن فعال، به سرعت رادیکالها را خنثی میکنند. با این حال، استفاده از آنها در محصولات پزشکی ممنوع است زیرا باعث تغییر رنگ شدید (لکه سیاه یا قهوهای) و سمیت احتمالی میشوند.
- فنولهای ممانعتشده (Hindered Phenols): (مانند BHT یا Irganox 1010) رایجترین آنتیرادها برای پلیمرهای پزشکی (مانند سرنگهای PP) هستند. اگرچه کارایی آنها کمی پایینتر از آمینهاست، اما مزیت بزرگ آنها عدم ایجاد تغییر رنگ شدید (Non-staining) و ایمنی فیزیولوژیک آنهاست.
۲. ترکیبات آروماتیک چندحلقهای
این دسته شامل موادی مانند آنتراسن، پیرن و فنانترن است. این ترکیبات به دلیل داشتن سیستم رزونانسی گسترده، گیرندههای عالی برای انتقال انرژی غیرتابشی هستند. افزودن مقدار کمی از این مواد به پلیمرهایی مانند PMMA (که شدیداً حساس است)، میتواند دوز آستانه تخریب را به طور قابل توجهی بالا ببرد. با این حال، ناسازگاری و مهاجرت این مواد به سطح، کاربرد آنها را محدود کرده است.
۳. گوگرد و ترکیبات آلی آن
عنصر گوگرد و ترکیبات حاوی آن (مانند تیولها و دیسولفیدها) محافظان بسیار موثری هستند. پیوند گوگرد-هیدروژن ($S-H$) ضعیف است و به راحتی هیدروژن خود را به رادیکال پلیمری میدهد تا آن را ترمیم کند. مشاهده میشود که ولکانیزاسیون لاستیک با گوگرد، خودبهخود مقاومت پرتویی آن را نسبت به پخت پراکسیدی افزایش میدهد.
۴. چالشهای انتخاب آنتیراد در صنعت
در انتخاب یک آنتیراد مناسب، تنها کارایی شیمیایی ملاک نیست. پارامترهای مهندسی زیر تعیینکننده هستند:
- سازگاری (Compatibility): آنتیراد باید در ماتریس پلیمر حل شود. اگر ناسازگار باشد، به سطح قطعه مهاجرت کرده (Blooming) و به صورت پودر سفید ظاهر میشود که در کاربردهای پزشکی غیرقابل پذیرش است.
- فراریت (Volatility): افزودنی نباید در دمای فرآورش (اکستروژن یا تزریق) یا در حین استریلیزاسیون تبخیر شود.
- سمیت و رنگ: در کاربردهای تماس با غذا و دارو، استفاده از آنتیرادهایی که محصولات جانبی سمی تولید میکنند یا باعث زرد شدن قطعه میشوند، مجاز نیست.