پلیمریزاسیون رادیکالی کنترل شده با نور
بسیاری از پژوهشگران در سنتز پلیمرهای پیشرفته با یک چالش بنیادی روبرو هستند: زمانی که پلیمریزاسیون حرارتی آغاز میشود، توقف آن در یک لحظه دقیق یا اعمال تغییرات آنی در معماری زنجیر تقریباً غیرممکن است. انرژی حرارتی فاقد آن سوئیچ «خاموش/روشن» است که برای طراحی مواد هوشمند و دقیق به آن نیاز داریم. این محدودیت، یک پرسش اساسی را ایجاد میکند: چگونه میتوانیم انرژی فعالسازی را از گرما جدا کنیم و در عوض، از محرکی استفاده کنیم که کنترل کامل زمانی و مکانی را بر رشد زنجیر پلیمری در اختیار ما قرار دهد؟
ما در این مقاله تخصصی، به بررسی مکانیسمهای پلیمریزاسیون رادیکالی کنترل شده با نور (Photo-CRP) میپردازیم تا پاسخی عملیاتی برای این نیاز ارائه دهیم. تمرکز اصلی ما بر واکاوی سینتیک انتقال الکترون در روش Photo-ATRP و تحلیل دقیق مکانیسمهای دوگانه در Photo-RAFT خواهد بود. هدف ما این است که مهندسان پلیمر و شیمیدانان با درک عمیق این روشهای نوری، بتوانند بر چالشهای سنتز ماکرومولکولهای پیچیده غلبه کنند و کنترل ساختاری را به سطحی بالاتر ارتقا دهند.
- مبانی فوتوفیزیکی و ترمودینامیک در پلیمریزاسیون نوری
- بررسی عمیق پلیمریزاسیون رادیکالی انتقال اتم نوری (Photo-ATRP)
- مهندسی دقیق پلیمریزاسیون RAFT تحت تابش نور (Photo-RAFT)
- کتابخانه فوتوکاتالیستها: دستهبندی، ساختار و عملکرد
- استراتژیهای پیشرفته تحمل اکسیژن
- سینتیک واکنش و کنترل زمانی (Temporal Control)
- معماریهای پیچیده و کاربردهای پیشرفته (Advanced Architectures)
- مهندسی راکتور و ملاحظات تجربی (Experimental Setup)
- مقایسه انتقادی و جدول تصمیمگیری (Critical Review)
- چشمانداز آینده و چالشهای باقیمانده
- پروتکل اجرایی استاندارد و ملاحظات ایمنی در آزمایشگاه
- پرسشهای متداول تخصصی (FAQ)
- ۱. تفاوت اصلی بین مکانیسم Photo-ATRP و Photo-RAFT در چیست؟
- ۲. آیا میتوانیم از هر نوع منبع نوری برای این واکنشها استفاده کنیم؟
- ۳. چرا پلیمریزاسیون من پس از چند دقیقه متوقف میشود (Dead Polymerization)؟
- ۴. چگونه میتوانم کاتالیست فلزی (مثلاً مس) را به طور کامل از محصول نهایی حذف کنم؟
- ۵. آیا سیستمهای Photo-CRP برای سنتز پلیمرهای زیستی (Bio-polymers) مناسب هستند؟
مبانی فوتوفیزیکی و ترمودینامیک در پلیمریزاسیون نوری
ما برای تحلیل دقیق فرآیندهای Photo-CRP، باید اصول فوتوفیزیکی حاکم بر سیستم را بررسی کنیم. در این واکنشها، فوتون به عنوان یک عامل شروعکننده عمل میکند که انرژی لازم برای غلبه بر سدهای انرژی اکتیواسیون را تأمین مینماید. در این بخش، ما مکانیزم جذب نور، تشکیل حالتهای برانگیخته و ترمودینامیک انتقال الکترون را که اساس تمامی روشهای پلیمریزاسیون نوری است، تشریح میکنیم.
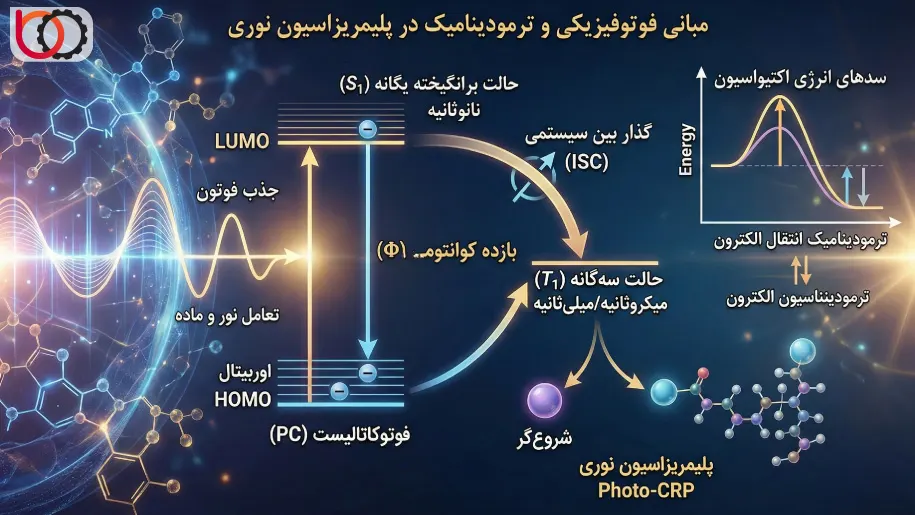
زمانی که محلول حاوی فوتوکاتالیست (PC) تحت تابش قرار میگیرد، جذب فوتون منجر به انتقال الکترونی از اوربیتال HOMO به LUMO میشود. طبق نمودار ژابلونسکی (Jablonski Diagram)، مولکول ابتدا به حالت برانگیخته یگانه ($S_1$) میرسد. طول عمر این حالت بسیار کوتاه (در محدوده نانوثانیه) است و برای انجام واکنشهای دو مولکولی کارآمد نیست.
ما در انتخاب کاتالیستهای مناسب برای پلیمریزاسیون، به دنبال ترکیباتی هستیم که بازده بالایی در «گذار بین سیستمی» (Intersystem Crossing – ISC) داشته باشند. این فرآیند به الکترون اجازه میدهد با تغییر اسپین، به حالت سهگانه ($T_1$) وارد شود. حالت سهگانه به دلیل ممنوعیتهای کوانتومی برای بازگشت مستقیم به حالت پایه، طول عمر بیشتری (میکروثانیه تا میلیثانیه) دارد. این پایداری زمانی به کاتالیست فرصت کافی میدهد تا نفوذ کرده و با شروعگر یا عامل انتقال زنجیر برهمکنش موثر داشته باشد. پارامتر سنجش کارایی در این مرحله، بازده کوانتومی ($\Phi$) است که نسبت مولکولهای واکنشداده به تعداد فوتونهای جذبشده را نشان میدهد.
سینتیک انتقال الکترون القا شده با نور (PET)
مکانیسم غالب در اکثر سیستمهای Photo-ATRP و PET-RAFT، فرآیند انتقال الکترون (Electron Transfer) است. ما برای تعیین امکانپذیری ترمودینامیکی این انتقال، از معادله رایم-ولر (Rehm-Weller Equation) استفاده میکنیم. این معادله تغییر انرژی آزاد گیبس ($\Delta G_{PET}$) را محاسبه میکند:
$$\Delta G_{PET} = E_{ox}(D) – E_{red}(A) – E_{0,0} + w_p$$
در این رابطه، $E_{ox}(D)$ پتانسیل اکسیداسیون دهنده الکترون، $E_{red}(A)$ پتانسیل احیای گیرنده الکترون، $E_{0,0}$ انرژی حالت برانگیخته کاتالیست و $w_p$ کار الکترواستاتیک (که در حلالهای قطبی معمولاً ناچیز است) میباشد.
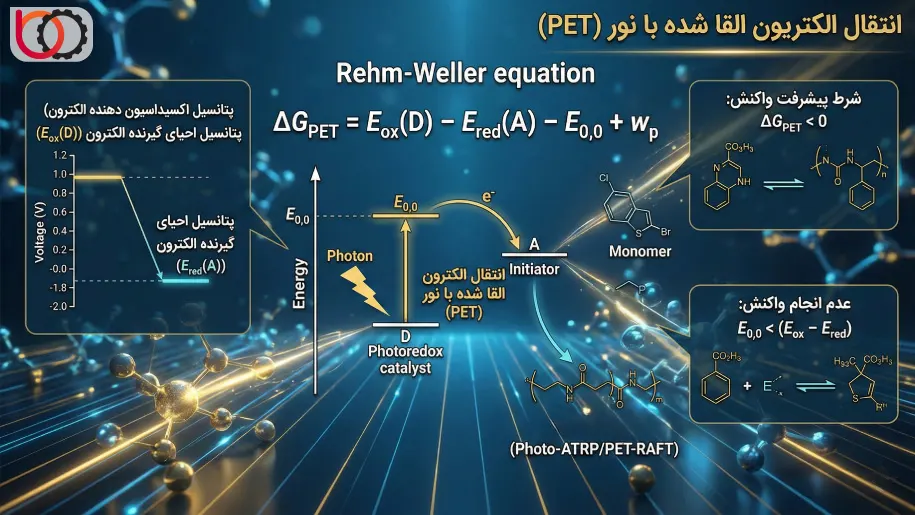
ما تنها در صورتی انتظار پیشرفت واکنش پلیمریزاسیون را داریم که مقدار $\Delta G_{PET}$ منفی باشد. این محاسبات به ما امکان میدهد تا جفت کاتالیست/شروعگر را پیش از آزمایش عملی انتخاب کنیم. اگر انرژی حالت برانگیخته ($E_{0,0}$) کمتر از اختلاف پتانسیل ردوکس باشد، انتقال الکترون رخ نمیدهد.
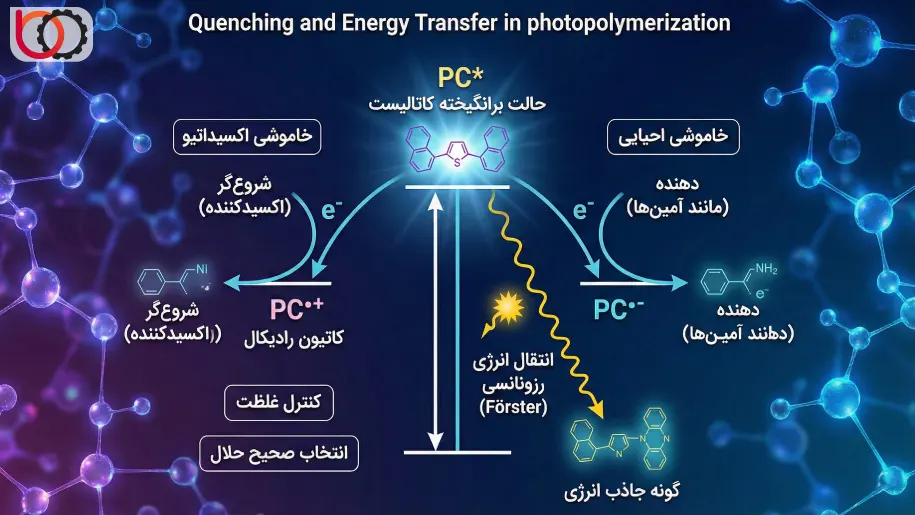
پدیده خاموشی (Quenching) و انتقال انرژی
در محیط واکنش، حالت برانگیخته کاتالیست ($PC^*$) ممکن است از طریق مسیرهای ناخواسته غیرفعال شود که به آن «خاموشی» میگوییم. ما دو مسیر اصلی خاموشی دینامیک را در نظر میگیریم:
۱. خاموشی اکسیداتیو: کاتالیست برانگیخته الکترون خود را به شروعگر (اکسیدکننده) منتقل میکند و خود به کاتیون رادیکال تبدیل میشود.
۲. خاموشی احیایی: کاتالیست ابتدا یک الکترون از یک دهنده (مانند آمینها یا برخی مونومرها) دریافت میکند.
علاوه بر انتقال الکترون، ما باید احتمال انتقال انرژی رزونانسی (مانند مکانیزم Förster) را نیز در نظر بگیریم. اگر گونههای جاذب دیگری در سیستم وجود داشته باشند که تراز انرژی آنها با کاتالیست همپوشانی دارد، انرژی بدون انتقال ماده منتقل شده و بازده واکنش افت میکند. کنترل غلظت و انتخاب صحیح حلال برای به حداقل رساندن این تلفات انرژی ضروری است.
بررسی عمیق پلیمریزاسیون رادیکالی انتقال اتم نوری (Photo-ATRP)
ما در این بخش، مکانیسم پلیمریزاسیون رادیکالی انتقال اتم نوری (Photo-ATRP) را به عنوان یکی از دقیقترین روشهای سنتز پلیمر بررسی میکنیم. در سیستمهای ATRP حرارتی سنتی، تعادل بین گونههای فعال (رادیکالها) و غیرفعال (زنجیرهای خوابیده) توسط گرما کنترل میشود. اما در Photo-ATRP، ما از انرژی فوتونی برای دستکاری این تعادل شیمیایی استفاده میکنیم که امکان انجام واکنش در دمای اتاق و حتی دماهای پایینتر را فراهم میآورد.
تکامل مکانیسمهای کاتالیستی
اساس Photo-ATRP بر پایه یک چرخه اکسیداسیون-احیاء (Redox) برگشتپذیر بنا شده است. در حالت کلی، یک کمپلکس فلز واسطه در حالت اکسایش پایین ($Mt^n$ – اکتیواتور) با یک هالید آلکیل ($R-X$) واکنش میدهد تا یک رادیکال کربن ($R^\bullet$) و یک کمپلکس فلزی در حالت اکسایش بالاتر ($X-Mt^{n+1}$ – دیاکتیواتور) تولید کند.
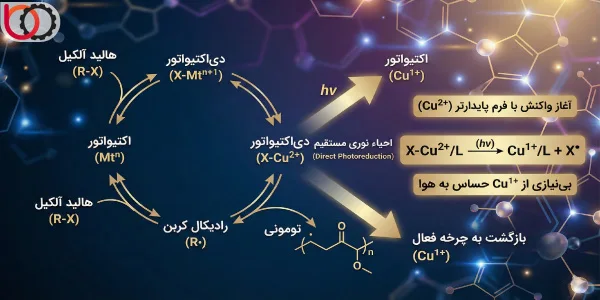
ما در روش نوری، با دو مکانیسم اصلی روبرو هستیم:
- احیاء نوری مستقیم (Direct Photoreduction): در این حالت، گونه دیاکتیواتور ($X-Cu^{II}$) که در سیستم تجمع مییابد، مستقیماً نور را جذب کرده و یا توسط یک حساسکننده نوری برانگیخته میشود تا دوباره به گونه اکتیواتور ($Cu^I$) احیاء شود.$$X-Cu^{II}/L \xrightarrow{h\nu} Cu^{I}/L + X^\bullet$$این فرآیند به ما اجازه میدهد تا واکنش را با فرم پایدارتر و ارزانتر مس ($Cu^{II}$) آغاز کنیم، در حالی که در روش حرارتی معمولاً نیازمند شروع با $Cu^I$ حساس به هوا هستیم.
سیستمهای Photo-ATRP کاتالیست فلزی (Metal-Catalyzed)
در این دسته از واکنشها، ما عمدتاً بر کمپلکسهای مس تمرکز داریم. انتخاب لیگاند ($L$) در اینجا بسیار حیاتیتر از روش حرارتی است، زیرا لیگاند نه تنها پتانسیل ردوکس را تنظیم میکند، بلکه خواص جذب نوری کمپلکس را نیز تعیین مینماید. ما معمولاً از لیگاندهای نیتروژنی چند دندانه مانند $TPMA$ یا $Me_6TREN$ استفاده میکنیم که پایداری بالایی در برابر تابش UV و نور مرئی دارند.
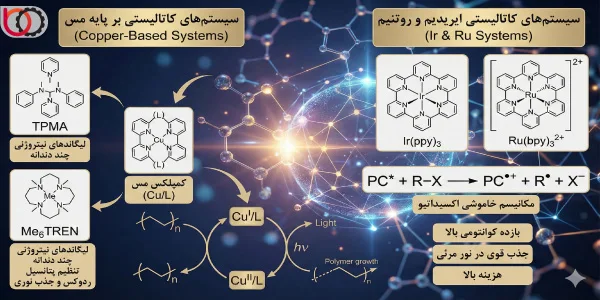
علاوه بر مس، ما از سیستمهای کاتالیستی بر پایه ایریدیم ($Ir(ppy)_3$) و روتنیم ($Ru(bpy)_3^{2+}$) نیز بهره میبریم. این کمپلکسها معمولاً از طریق یک مکانیسم «خاموشی اکسیداتیو» عمل میکنند:
$$PC^* + R-X \rightarrow PC^{\bullet+} + R^\bullet + X^-$$
در این چرخه، فوتوکاتالیست ($PC$) الکترون را به هالید آلکیل منتقل میکند. مزیت اصلی استفاده از این فلزات نجیب، بازده کوانتومی بسیار بالا و جذب قوی در ناحیه نور مرئی است، هرچند هزینه بالای آنها کاربرد صنعتی را محدود میکند.
پدیده Photo-induced Metal-Free ATRP (تکنولوژی O-ATRP)
یکی از مهمترین پیشرفتهای اخیر که ما در تحقیقات خود بر آن تمرکز داریم، حذف کامل فلز از سیستم و جایگزینی آن با فوتوکاتالیستهای آلی (Organic Photocatalysts) است که به آن O-ATRP میگوییم. در این روش، مولکولهایی مانند فنوتیازینها (Phenothiazines)، پریلن (Perylene) و مشتقات دیهیدروفنازین نقش کاتالیست را ایفا میکنند.
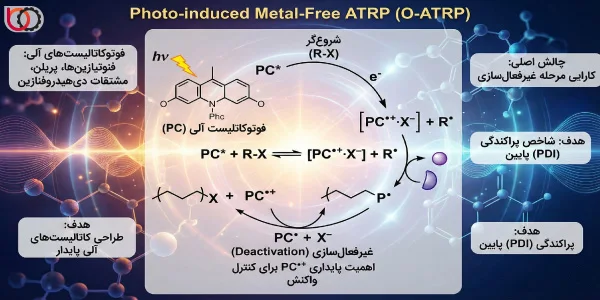
مکانیسم O-ATRP متفاوت از همتایان فلزی خود است. پس از برانگیختگی کاتالیست آلی ($PC^*$) و انتقال الکترون به شروعگر ($R-X$)، یک جفتیون (Ion-Pair) شامل کاتیون رادیکال کاتالیست ($PC^{\bullet+}$) و آنیون هالید ($X^-$) تشکیل میشود:
$$PC^* + R-X \rightleftharpoons [PC^{\bullet+} \cdot X^-] + R^\bullet$$
چالش اصلی که ما در O-ATRP با آن مواجهیم، کارایی مرحله غیرفعالسازی (Deactivation) است. برای داشتن یک پلیمر با شاخص پراکندگی (PDI) پایین، کاتیون رادیکال $PC^{\bullet+}$ باید بتواند به سرعت با رادیکال در حال رشد ($P^\bullet$) واکنش داده و اتم هالوژن را به آن بازگرداند. اگر $PC^{\bullet+}$ ناپایدار باشد و تجزیه شود، کنترل واکنش از دست رفته و پلیمریزاسیون به سمت مکانیسم رادیکال آزاد (FRP) منحرف میشود. بنابراین، طراحی مولکولی کاتالیستهای آلی پایدار، اولویت اصلی در توسعه O-ATRP است.
مهندسی دقیق پلیمریزاسیون RAFT تحت تابش نور (Photo-RAFT)
ما در این بخش به سراغ یکی از منعطفترین روشهای پلیمریزاسیون رادیکالی غیرفعالسازی برگشتپذیر، یعنی پلیمریزاسیون انتقال زنجیر افزایشی-قطعهقطعهشدن (RAFT) میرویم و رفتار آن را تحت تابش نور بررسی میکنیم. در حالی که RAFT حرارتی به یک منبع تولید رادیکال خارجی (مثل AIBN) نیاز دارد، در Photo-RAFT ما از نور برای تولید رادیکالها یا فعالسازی مستقیم عامل انتقال زنجیر (CTA) استفاده میکنیم. این رویکرد به ما امکان میدهد تا کنترل وزن مولکولی و توزیع آن (PDI) را با دقتی فراتر از روشهای حرارتی انجام دهیم.
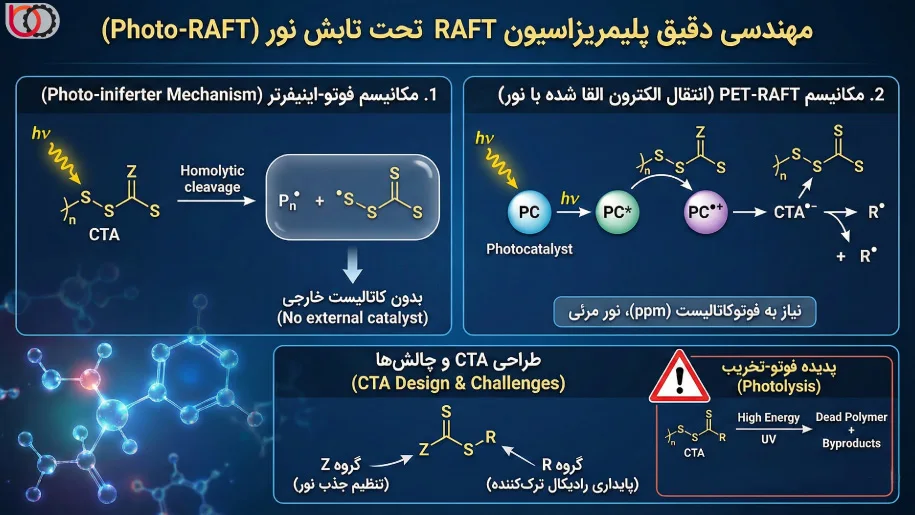
دوگانگی مکانیسم: Iniferter vs PET-RAFT
ما در سیستمهای Photo-RAFT با دو مسیر مکانیسمی کاملاً متفاوت روبرو هستیم که تفکیک آنها برای طراحی آزمایش حیاتی است:
۱. مکانیسم فوتو-اینیفرتر (Photo-iniferter):
در این روش، خودِ عامل CTA (معمولاً تریتیوکربناتها یا دیتیواسترها) نقش جاذب نور را بازی میکند. با جذب فوتون، پیوند ضعیف کربن-گوگرد ($C-S$) در عامل RAFT دچار شکست هومولیتیک میشود:
$$P_n-S-C(Z)=S \xrightarrow{h\nu} P_n^\bullet + ^\bullet S-C(Z)=S$$
ما در اینجا نیازی به کاتالیست یا شروعگر خارجی نداریم. رادیکال پلیمری ($P_n^\bullet$) رشد میکند و رادیکال تیوکربنیل ($^\bullet S-C(Z)=S$) به عنوان گونه پایدارکننده عمل میکند. با قطع نور، این دو رادیکال مجدداً ترکیب شده و واکنش بلافاصله متوقف میشود.
۲. مکانیسم PET-RAFT (انتقال الکترون القا شده با نور):
در این سناریو، ما از یک فوتوکاتالیست خارجی ($PC$) استفاده میکنیم که نور مرئی را جذب میکند. کاتالیست برانگیخته ($PC^*$) یک الکترون به عامل CTA منتقل میکند و آن را به آنیون رادیکال کاهش میدهد:
$$PC^* + CTA \rightarrow PC^{\bullet+} + CTA^{\bullet-}$$
سپس $CTA^{\bullet-}$ قطعهقطعه شده و رادیکال فعال را آزاد میکند. ما در PET-RAFT میتوانیم با استفاده از مقادیر بسیار کم کاتالیست (در حد ppm)، واکنش را در طول موجهایی انجام دهیم که خود عامل RAFT جذبی ندارد.
طراحی عوامل انتقال زنجیر (CTA) مخصوص نور
موفقیت ما در Photo-RAFT مستقیماً به ساختار شیمیایی عامل انتقال زنجیر (CTA) بستگی دارد. این عوامل معمولاً ساختار عمومی $Z-C(=S)S-R$ را دارند.
- گروه Z (تنظیمکننده): این گروه نه تنها واکنشپذیری پیوند $C=S$ را تعیین میکند، بلکه در Photo-RAFT مسئول اصلی جذب نور است. برای مثال، ما با انتخاب گروههای فنیل (در دیتیوبنزواتها)، جذب را به ناحیه مرئی شیفت میدهیم، در حالی که گروههای آلکیل (در تریتیوکربناتها) بیشتر در ناحیه UV فعال هستند.
- گروه R (گروه ترککننده): این گروه باید به گونهای باشد که رادیکال حاصل ($R^\bullet$) پایداری کافی برای شروع مجدد پلیمریزاسیون را داشته باشد. ما در طراحی آزمایش باید تطابق پتانسیل ردوکس گروه $R$ با کاتالیست انتخابی را در نظر بگیریم تا چرخه انتقال الکترون مختل نشود.
پدیده فوتو-تخریب (Photolysis) عوامل RAFT
یکی از چالشهای فنی که ما در آزمایشگاه با آن مواجه میشویم، پایداری عامل RAFT در برابر تابش طولانیمدت است. اگر انرژی فوتونها بیش از حد زیاد باشد (مانند UV کوتاه)، ممکن است واکنشهای جانبی رخ دهد که منجر به گوگردزدایی (Desulfurization) یا تخریب کامل گروه تیوکربنیل شود.
$$CTA \xrightarrow{High Energy UV} Dead Polymer + Byproducts$$
این تخریب باعث از بین رفتن خاصیت «زنده» بودن پلیمر میشود، به طوری که زنجیرها دیگر قابلیت رشد مجدد ندارند. برای حل این مشکل، ما استراتژیهای خود را به سمت استفاده از نورهای کمانرژیتر (مانند نور سبز یا قرمز) و استفاده از کاتالیستهای PET که در طول موجهای ایمن عمل میکنند، تغییر میدهیم. این کار بقای گروه انتهایی RAFT را برای مراحل بعدی (مانند سنتز کوپلیمرهای قطعهای) تضمین میکند.
کتابخانه فوتوکاتالیستها: دستهبندی، ساختار و عملکرد
ما در طراحی یک سیستم پلیمریزاسیون نوری کارآمد، با انتخاب حیاتی فوتوکاتالیست (PC) روبرو هستیم. این مولکولها به عنوان مبدلهای انرژی عمل میکنند که فوتونهای فرودی را به پتانسیل شیمیایی الکتروشیمیایی ترجمه مینمایند. برخلاف روشهای حرارتی که انتخاب آغازگر محدود است، در Photo-CRP ما با طیف گستردهای از کاتالیستها با پنجرههای پتانسیل ردوکس ($E_{redox}$) و ضرایب جذب مولی ($\epsilon$) متفاوت سروکار داریم. در این بخش، ما دستهبندیهای اصلی و اصول رابطه ساختار-خاصیت (SAR) در آنها را بررسی میکنیم.
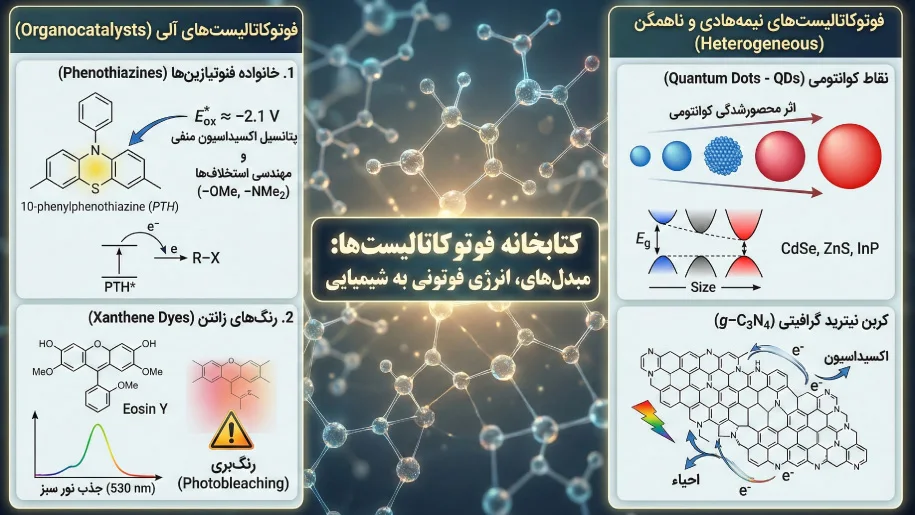
فوتوکاتالیستهای آلی (Organocatalysts)
تمرکز عمده ما در توسعه روشهای مدرن، حذف فلزات واسطه و حرکت به سمت O-ATRP یا PET-RAFT تمام آلی است. این رویکرد برای کاربردهای زیستپزشکی که حد مجاز فلزات (ppm) بسیار سختگیرانه است، اهمیت دارد.
۱. خانواده فنوتیازینها (Phenothiazines):
ترکیباتی مانند ۱۰-فنیلفنوتیازین ($PTH$) ستون اصلی کاتالیستهای کاهنده شدید هستند. این مولکولها در حالت برانگیخته پتانسیل اکسیداسیون ($E^*_{ox}$) بسیار منفی (حدود $-2.1 V$ نسبت به SCE) دارند که آنها را قادر میسازد حتی غیرفعالترین پیوندهای کربن-هالوژن را احیاء کنند. ما با مهندسی استخلافهای روی حلقه آروماتیک (مثلاً افزودن گروههای الکتروندهنده مانند $-OMe$ یا $-NMe_2$)، میتوانیم پایداری کاتیون رادیکال تشکیل شده ($PC^{\bullet+}$) را افزایش داده و بازده واکنش را بهبود بخشیم.
۲. رنگهای زانتن (Xanthene Dyes):
مولکولهایی نظیر ائوزین Y ($Eosin Y$)، رز بنگال و فلورسین، گزینههای استاندارد ما برای پلیمریزاسیون تحت تابش نور مرئی (به ویژه نور سبز ۵۳۰ نانومتر) هستند. این رنگها معمولاً از طریق مکانیسم اکسیداتیو در سیکل کاتالیستی شرکت میکنند. با این حال، ما باید در نظر داشته باشیم که این رنگها پایداری نوری کمتری نسبت به فنوتیازینها دارند و ممکن است در طول واکنشهای طولانی دچار پدیده رنگبری (Photobleaching) شوند.
فوتوکاتالیستهای نیمههادی و ناهمگن (Heterogeneous)
ما برای حل چالش جداسازی کاتالیست از محصول پلیمری، از سیستمهای کاتالیستی فاز جامد استفاده میکنیم. این مواد نامحلول پس از اتمام پلیمریزاسیون با سانتریفیوژ یا فیلتراسیون ساده جدا شده و قابل استفاده مجدد هستند.
- نقاط کوانتومی (Quantum Dots – QDs): نانوکریستالهای نیمههادی کلوئیدی (مانند $CdSe$، $ZnS$ یا $InP$) که ویژگی بارز آنها اثر محصورشدگی کوانتومی (Quantum Confinement) است. ما با تغییر اندازه هسته این ذرات، میتوانیم شکاف باند انرژی ($E_g$) و در نتیجه طول موج جذب را دقیقاً تنظیم کنیم.
- کربن نیترید گرافیتی ($g-C_3N_4$): یک پلیمر نیمههادی دوبعدی و بدون فلز که پایداری شیمیایی و حرارتی بالایی دارد. ما از این ماده به عنوان یک کاتالیست سبز تحت نور مرئی استفاده میکنیم که قادر است هم در اکسیداسیون و هم در احیای گونههای پلیمری شرکت کند.
استراتژیهای پیشرفته تحمل اکسیژن
ما در اجرای عملی پلیمریزاسیون رادیکالی، همواره با یک دشمن نامرئی اما قدرتمند روبرو هستیم: اکسیژن اتمسفری. در روشهای سنتی، ما مجبور به استفاده از تکنیکهای پرزحمت گاززدایی فیزیکی (مانند چرخه انجماد-تخلیه-ذوب یا دمیدن گاز بیاثر) هستیم تا غلظت اکسیژن را به زیر ppm برسانیم. اما در نسل جدید سیستمهای Photo-CRP، ما رویکرد متفاوتی را اتخاذ میکنیم: به جای حذف فیزیکی اکسیژن، از شیمی نور برای تبدیل یا مصرف آن در محیط واکنش استفاده میکنیم تا به پارادایم «ظرف-باز» (Open-to-Air) دست یابیم.
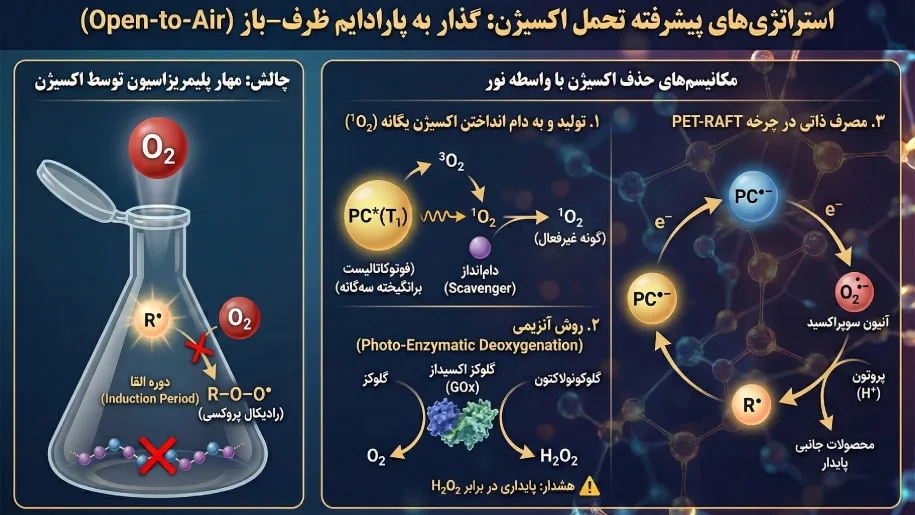
پارادایم “Open-to-Air” در سنتز پلیمر
چالش اصلی حضور اکسیژن، واکنشپذیری فوقالعاده بالای آن با رادیکالهای کربنی فعال ($R^\bullet$) است. سرعت این واکنش محدودکننده نفوذ ($k \approx 10^9 M^{-1}s^{-1}$) بسیار بیشتر از سرعت انتشار پلیمریزاسیون ($k_p$) است.
$$R^\bullet + O_2 \rightarrow R-O-O^\bullet$$
رادیکال پروکسی تشکیل شده ($R-O-O^\bullet$) نسبتاً پایدار است و قادر به ادامه زنجیر نیست. این پدیده باعث ایجاد یک «دوره القا» (Induction Period) میشود که در آن تا زمانی که تمام اکسیژن محلول مصرف نشود، پلیمریزاسیون آغاز نخواهد شد. ما در سیستمهای نوری، به دنبال راهکارهایی هستیم که این دوره را حذف کرده یا به حداقل برسانیم بدون اینکه نیازی به تجهیزات خلأ باشد.
مکانیسمهای حذف اکسیژن با واسطه نور
ما در اینجا سه استراتژی شیمایی-نوری اصلی را برای غلبه بر این مشکل به کار میگیریم:
۱. تولید اکسیژن یگانه ($^1O_2$) و به دام انداختن آن:
بسیاری از فوتوکاتالیستهای ما (به ویژه رنگهای آلی مانند ائوزین Y) میتوانند انرژی حالت سهگانه خود را به اکسیژن محلول (که در حالت پایه سهگانه است) منتقل کنند. این انتقال انرژی باعث تولید اکسیژن یگانه ($^1O_2$) میشود:
$$PC^*(T_1) + ^3O_2 \rightarrow PC(S_0) + ^1O_2$$
اکسیژن یگانه بسیار واکنشپذیر است و ما با افزودن یک “Scavenger” یا دامانداز (مانند حلال دیمتیل سولفوکسید یا آنتراسن)، آن را سریعاً به یک گونه غیررادیکالی و بیخطر تبدیل میکنیم. این فرآیند به طور مداوم اکسیژن را از محیط حذف میکند.
۲. روش آنزیمی (Photo-Enzymatic Deoxygenation):
در یک رویکرد بیوهیبریدی، ما از آنزیم گلوکز اکسیداز (GOx) در کنار سیستم نوری استفاده میکنیم. در حضور گلوکز، این آنزیم اکسیژن محلول را مصرف کرده و به هیدروژن پروکسید تبدیل میکند. اگرچه این روش بسیار موثر است، اما ما باید پایداری کاتالیست نوری را در برابر پروکسید تولید شده ($H_2O_2$) در نظر بگیریم.
۳. مصرف ذاتی در چرخه PET-RAFT:
در برخی سیستمهای پیشرفته PET-RAFT، ما مشاهده میکنیم که اکسیژن به عنوان بخشی از چرخه کاتالیستی مصرف میشود. کاتالیست احیاء شده ($PC^{\bullet-}$) میتواند الکترون را به اکسیژن منتقل کرده و آن را به آنیون سوپراکسید ($O_2^{\bullet-}$) تبدیل کند. این آنیون سپس توسط پروتونهای محیط یا سایر افزودنیها خنثی میشود. این مکانیسم خودتنظیمگر به ما اجازه میدهد حتی در مقادیر بسیار کمِ کاتالیست (ppm)، بر مهار اکسیژن غلبه کنیم.
سینتیک واکنش و کنترل زمانی (Temporal Control)
ما در تحلیل فرآیندهای Photo-CRP، تنها به محصول نهایی اکتفا نمیکنیم؛ بلکه رفتار دینامیک سیستم در طول زمان برای ما اهمیت حیاتی دارد. ویژگی منحصربهفرد نور به عنوان یک محرک بدون جرم، به ما این امکان را میدهد که سرعت واکنش ($R_p$) را به صورت آنی و با دقت بالا مدولاسیون کنیم. در این بخش، ما سینتیک پلیمریزاسیون و وابستگیهای ریاضی آن به پارامترهای تابش را بررسی میکنیم.
تحلیل آزمایشهای “روشن/خاموش” (On/Off Experiments)
معیار طلایی ما برای اثبات ماهیت «کنترلشدگی» و «زنده بودن» یک سیستم پلیمری، آزمایشهای متناوب نوری است. در یک سیستم ایدهآل Photo-ATRP یا Photo-RAFT، ما انتظار داریم که با تابش نور، غلظت گونههای رادیکال فعال ($[P^\bullet]$) به سرعت به حالت پایدار برسد و پلیمریزاسیون آغاز شود. به محض قطع نور، بازترکیب یا غیرفعالسازی سریع رادیکالها باید منجر به توقف کامل مصرف مونومر شود.
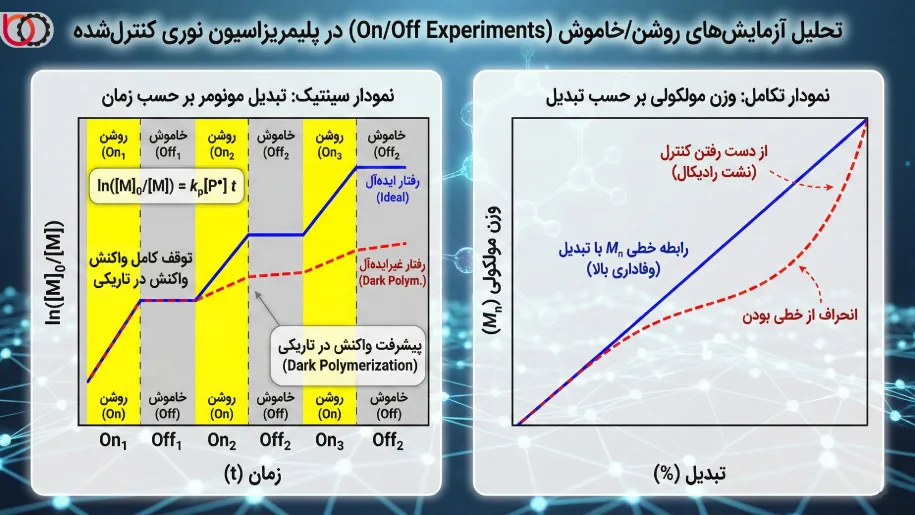
ما دادههای حاصل را با رسم نمودار نیمهلگاریتمی تبدیل مونومر ($ln([M]_0/[M])$) بر حسب زمان ($t$) تحلیل میکنیم.
$$\ln \left( \frac{[M]_0}{[M]} \right) = k_p [P^\bullet] t$$
در بازههای زمانی «روشن»، شیب نمودار خطی است که نشاندهنده ثابت بودن غلظت رادیکالها ($[P^\bullet]$) و سینتیک درجه اول کاذب نسبت به مونومر است. در بازههای «خاموش»، شیب باید دقیقاً صفر شود (خط افقی). اگر ما در بازههای تاریکی همچنان شاهد پیشرفت واکنش باشیم (Dark Polymerization)، این نشاندهنده نشت رادیکال یا نرخ پایین غیرفعالسازی ($k_{deact}$) است که کنترل وزن مولکولی را مختل میکند. وفاداری (Fidelity) بالای سیستم زمانی اثبات میشود که پس از چندین چرخه روشن/خاموش، نمودار تکامل وزن مولکولی ($M_n$) بر حسب درصد تبدیل همچنان خطی باقی بماند.
تاثیر شدت نور ($I_0$) بر سرعت پلیمریزاسیون ($R_p$)
یکی از متغیرهای قابل تنظیم که ما برای کنترل سرعت واکنش در اختیار داریم، شدت تابش منبع نور ($I_0$) است. رابطه بین سرعت پلیمریزاسیون و شدت نور معمولاً از یک قانون توانی (Power Law) پیروی میکند:
$$R_p \propto I_0^\alpha$$
در تئوری کلاسیک رادیکال آزاد، اگر اختتام زنجیرها صرفاً از طریق جفتشدن دو رادیکال (Bimolecular Termination) باشد، توان $\alpha$ برابر با $0.5$ است. اما ما در سیستمهای Photo-CRP پیچیده، بسته به مکانیسم غالب (مانند محدودیت انتقال جرم یا جذب نوری رقابتی)، مقادیری بین $0.5$ تا $1.0$ را مشاهده میکنیم.
ما همچنین باید پدیده «اشباع نوری» (Optical Saturation) را در نظر بگیریم. در شدتهای بسیار بالا، سرعت تولید رادیکال ممکن است از ظرفیت کاتالیست برای غیرفعالسازی فراتر رود، یا غلظت رادیکالها به حدی برسد که واکنشهای جانبی و اختتام زنجیر بر رشد غلبه کنند. علاوه بر این، طبق قانون لامبرت-بیر، با افزایش غلظت کاتالیست یا ضخامت ظرف واکنش، نفوذ نور کاهش مییابد. این امر منجر به ایجاد گرادیان غلظت رادیکال در عمق ظرف میشود که میتواند توزیع وزن مولکولی (PDI) را پهن کند.
معماریهای پیچیده و کاربردهای پیشرفته (Advanced Architectures)
ما در این مرحله از بحث، فراتر از کنترل وزن مولکولی ساده میرویم و بر توانایی منحصربهفرد نور در «مجسمهسازی مولکولی» تمرکز میکنیم. برخلاف روشهای حرارتی که کل حجم واکنش را به صورت یکنواخت تحت تأثیر قرار میدهند، ما در سیستمهای Photo-CRP از ویژگیهای برداری نور برای ایجاد ساختارهایی استفاده میکنیم که پیش از این غیرممکن یا بسیار دشوار بودند. در این بخش، ما چگونگی بهرهگیری از این ابزار برای مهندسی سطوح و سنتز توپولوژیهای پیچیده پلیمری را بررسی میکنیم.
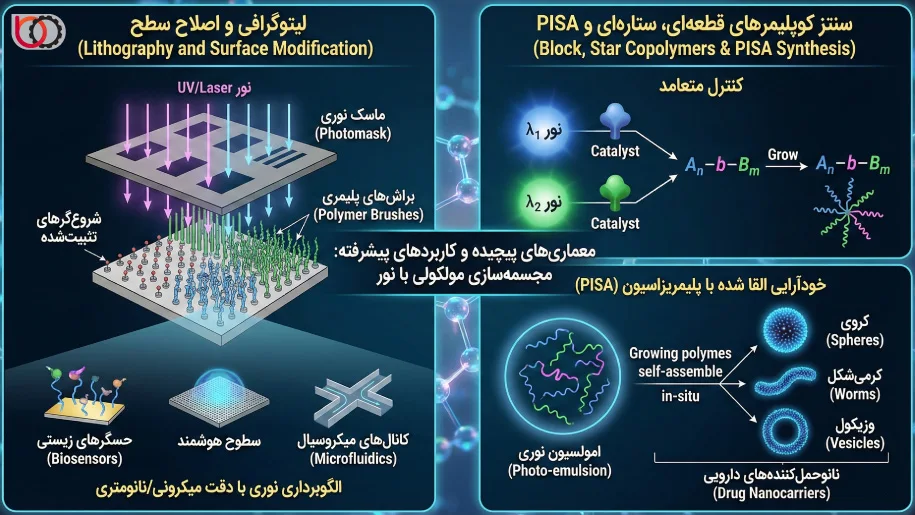
لیتوگرافی و اصلاح سطح (Surface-Initiated Photo-CRP)
یکی از قدرتمندترین کاربردهایی که ما با استفاده از پلیمریزاسیون نوری توسعه دادهایم، رشد پلیمر از سطح (SI-Photo-CRP) با دقت مکانی میکرونی و نانومتری است. در این فرآیند، ما ابتدا شروعگرهای ATRP یا عوامل RAFT را روی یک بستر جامد (مانند ویفرهای سیلیکونی، نانوذرات طلا یا شیشه) تثبیت میکنیم (Grafting-from).
سپس با تابش نور از طریق یک ماسک نوری (Photomask) یا استفاده از لیزر متمرکز، واکنش پلیمریزاسیون را تنها در مناطق نوردهی شده فعال میکنیم. این تکنیک که «الگوبرداری نوری» (Photopatterning) نامیده میشود، به ما اجازه میدهد تا «براشهای پلیمری» (Polymer Brushes) را با ارتفاع و چگالی متغیر در نقاط مختلف سطح رشد دهیم.
رابطه مستقیم بین زمان تابش و طول زنجیر در سیستمهای زنده، به ما این امکان را میدهد که توپوگرافی سطح را به صورت سهبعدی کنترل کنیم. ما از این روش برای ساخت حسگرهای زیستی، سطوح هوشمند پاسخگو و کانالهای میکروسیال (Microfluidics) با خواص شیمیایی سطحِ قابل تنظیم استفاده میکنیم.
سنتز کوپلیمرهای قطعهای (Block Copolymers) و ستارهای
ما در سنتز کوپلیمرهای قطعهای ($A_n-b-B_m$)، از ماهیت «زنده» بودن انتهای زنجیر در Photo-CRP بهره میبریم. پس از تکمیل پلیمریزاسیون مونومر اول ($A$) و مصرف کامل آن، ما میتوانیم مونومر دوم ($B$) را اضافه کرده و با تابش مجدد نور، رشد زنجیر را از سر بگیریم.
یک استراتژی پیشرفتهتر که ما به کار میگیریم، «کنترل متعامد» (Orthogonal Control) است. در این روش، ما از دو سیستم کاتالیستی یا شروعگر متفاوت استفاده میکنیم که هر کدام به طول موج خاصی ($\lambda_1$ و $\lambda_2$) حساس هستند. این به ما اجازه میدهد تا پلیمریزاسیون دو بلوک مختلف را به صورت مستقل و انتخابی با تغییر رنگ نور کنترل کنیم.
علاوه بر ساختارهای خطی، ما از این تکنیکها در محیطهای پراکنده (مانند امولسیون نوری) برای تولید نانوذرات پلیمری با مورفولوژیهای پیچیده استفاده میکنیم. در فرآیند «خودآرایی القا شده با پلیمریزاسیون» (PISA)، زنجیرها در حین رشد، تغییر حلالپوشی داده و به صورت درجا (In-situ) به ساختارهای کروی، کرمیشکل یا وزیکول تبدیل میشوند. این روش مسیر ما را برای تولید نانوحملکنندههای دارویی بدون نیاز به مراحل خالصسازی پیچیده هموار میکند.
مهندسی راکتور و ملاحظات تجربی (Experimental Setup)
ما در گذار از مقیاس میلیگرمی آزمایشگاهی به تولید گرمی و صنعتی، با چالشهای مهندسی روبرو هستیم که فراتر از شیمی مولکولی است. موفقیت یک واکنش Photo-CRP تنها به کاتالیست و مونومر وابسته نیست، بلکه هندسه راکتور و ویژگیهای فیزیکی منبع نور نقش تعیینکننده ای در یکنواختی و بازده نهایی ایفا میکنند. در این بخش، ما پارامترهای سختافزاری و تنظیمات تجربی لازم برای دستیابی به نتایج تکرارپذیر را بررسی میکنیم.
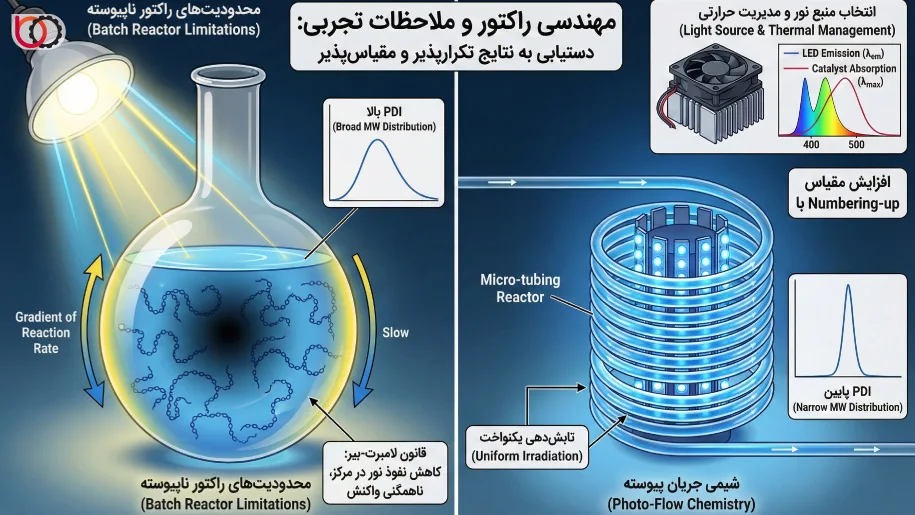
انتخاب منبع نور و تطبیق طیفی
نخستین گام مهندسی که ما برمیداریم، انتخاب منبع نور مناسب است. لامپهای جیوه یا زنون قدیمی به دلیل تولید حرارت زیاد و طیف گسترده، جای خود را به دیودهای ساطعکننده نور (LED) دادهاند. مزیت LEDها در تکفام بودن (Monochromaticity) نسبی آنهاست. ما باید طول موج نشر LED ($\lambda_{em}$) را دقیقاً با قله جذب فوتوکاتالیست ($\lambda_{max}$) همپوشانی دهیم.
پارامتر مهم دیگری که ما محاسبه میکنیم، شار فوتونی (Photon Flux) است که شدت نور موثر را تعیین میکند. ما نباید صرفاً به توان الکتریکی (وات) منبع نور تکیه کنیم، بلکه تابشسنجی (Radiometry) دقیق برای اندازهگیری شدت نور ($mW/cm^2$) در سطح راکتور ضروری است. همچنین، مدیریت حرارتی منبع نور حیاتی است؛ زیرا افزایش دما میتواند پارامترهای سینتیکی (مانند $k_p$ و $k_t$) را تغییر دهد و کنترل وزن مولکولی را مختل کند. بنابراین، ما همواره از سیستمهای خنککننده (Heat Sink) و فنهای قوی در کنار منبع نوری استفاده میکنیم تا شرایط همدما (Isothermal) حفظ شود.
شیمی جریان پیوسته (Photo-Flow Chemistry)
یکی از محدودیتهای ذاتی که ما در راکتورهای ناپیوسته (Batch) با آن مواجهیم، قانون لامبرت-بیر است. با افزایش حجم ظرف و غلظت کاتالیست، نفوذ نور به مرکز ظرف به شدت کاهش مییابد ($A = \varepsilon \cdot l \cdot c$). این امر باعث ایجاد گرادیان سرعت واکنش میشود؛ به طوری که واکنش در جدارهها سریع و در مرکز کند است. این ناهمگنی منجر به پهن شدن توزیع وزن مولکولی (PDI بالا) میشود.
ما برای حل این مشکل مهندسی، از راکتورهای جریان پیوسته (Flow Reactors) استفاده میکنیم. در این سیستمها، محلول واکنش از درون لولههایی با قطر کم (Micro-tubing) عبور میکند که دور منبع نور پیچیده شدهاند. این طراحی نسبت سطح به حجم ($S/V$) را به شدت افزایش میدهد و مسیر نوری ($l$) را کوتاه میکند.
در نتیجه، ما تابشدهی یکنواخت را در تمام حجم سیال تضمین میکنیم. علاوه بر این، سیستمهای جریان پیوسته امکان افزایش مقیاس (Scale-up) را از طریق “Numbering-up” (موازی کردن چندین راکتور) بدون تغییر شرایط واکنش فراهم میکنند، که مسیر اصلی ما برای صنعتیسازی Photo-CRP است.
مقایسه انتقادی و جدول تصمیمگیری (Critical Review)
ما اکنون با درک عمیق از هر دو مکانیسم Photo-ATRP و Photo-RAFT، به مرحله حساس انتخاب روش مناسب برای یک پروژه تحقیقاتی یا صنعتی میرسیم. واقعیت این است که هیچ روش واحدی برای تمام کاربردها بهینه نیست. ما باید بر اساس محدودیتهای مونومر، خلوص مورد نیاز محصول نهایی و امکانات آزمایشگاهی، بین این دو تکنیک مصالحه کنیم. در این بخش، ما یک تحلیل مقایسهای بیطرفانه را برای کمک به تصمیمگیری مهندسی ارائه میدهیم.
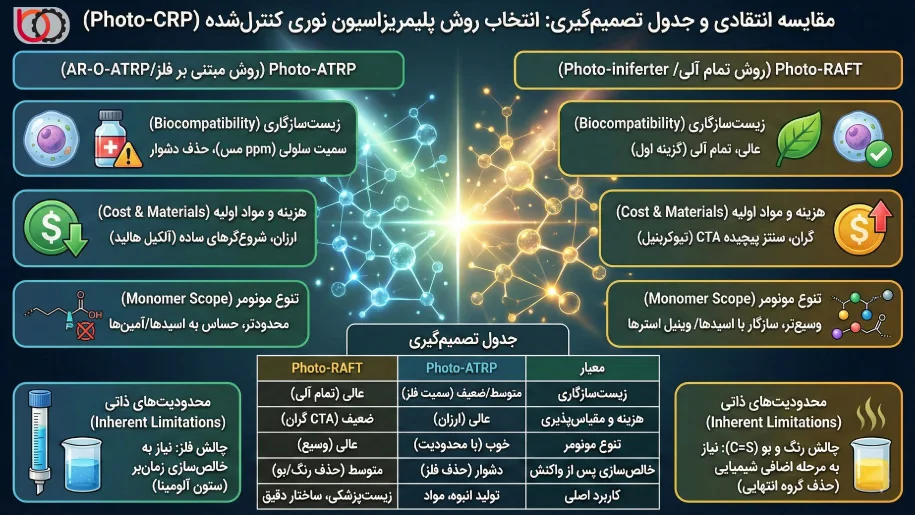
نبرد تکنیکها: Photo-ATRP در برابر Photo-RAFT
ما معیار انتخاب را بر اساس سه پارامتر کلیدی «زیستسازگاری»، «هزینه مواد اولیه» و «تنوع مونومر» ارزیابی میکنیم:
۱. کاربردهای زیستی (Bioconjugation):
در سنتز ترکیبات اتصالیافته به پروتئین یا دارو، اولویت ما عدم حضور فلزات سنگین سمی است. سیستمهای Photo-RAFT (بهویژه انواع بدون کاتالیست یا پلیمریزاسیون فوتو-اینیفرتر) به دلیل ماهیت تمام آلی، گزینه اول ما محسوب میشوند. اگرچه O-ATRP (روش بدون فلز) در حال توسعه است، اما بسیاری از سیستمهای Photo-ATRP کارآمد همچنان به مقادیر کمی (ppm) از مس نیاز دارند که سمیت سلولی (Cytotoxicity) دارد و حذف کامل آن دشوار است.
۲. هزینه و دسترسی به مواد:
از دیدگاه اقتصادی، Photo-ATRP دست برتر را دارد. شروعگرهای این روش (آلکیل هالیدها) ارزان هستند و به سادگی سنتز میشوند. در مقابل، عوامل انتقال زنجیر (CTA) در روش Photo-RAFT ترکیبات آلی گوگردی پیچیدهای هستند که سنتز چندمرحلهای دارند و هزینه تجاری آنها بسیار بالاست. بنابراین، ما برای تولید در مقیاس بالا (Scale-up)، اغلب به سمت ATRP متمایل میشویم مگر اینکه کنترل خاصی مدنظر باشد که فقط RAFT ارائه میدهد.
۳. دامنه مونومرها (Monomer Scope):
ما در Photo-RAFT با طیف وسیعتری از مونومرها آزادی عمل داریم. این روش برای مونومرهای حاوی گروههای عاملی اسیدی (مانند اکریلیک اسید) یا وینیل استرها (مانند وینیل استات) بسیار مناسب است. در مقابل، در Photo-ATRP مبتنی بر فلز، گروههای اسیدی میتوانند لیگاند کاتالیست را پروتونه کرده و کمپلکس را تخریب کنند، یا برخی آمینها میتوانند با جابجایی لیگاند، کاتالیست را غیرفعال نمایند.
محدودیتهای ذاتی هر روش
ما در کنار مزایا، باید چالشهای خالصسازی (Post-polymerization Processing) را نیز مدیریت کنیم:
- چالش فلز در ATRP: حتی با کاهش غلظت کاتالیست به ppm در روشهای نوری، محصول نهایی ممکن است همچنان رنگ آبی/سبز ضعیفی داشته باشد. ما برای کاربردهای الکترونیک نوری (Optoelectronics) که خلوص دیالکتریک حیاتی است، مجبور به استفاده از ستونهای آلومینا یا رزینهای تبادل یونی برای حذف کامل فلز هستیم که فرایندی زمانبر است.
- چالش رنگ و بو در RAFT: پلیمرهای حاصل از Photo-RAFT، به دلیل وجود گروه تیوکربنیل ($C=S$) در انتهای زنجیر، معمولاً رنگی (زرد تا صورتی) هستند و بوی نامطبوع ترکیبات گوگردی را دارند. علاوه بر این، این گروه انتهایی ممکن است در طول زمان ناپایدار باشد. ما اغلب مجبوریم یک مرحله اضافی شیمیایی (مانند آمینولیز یا اکسیداسیون) را برای حذف یا تبدیل گروه انتهایی انجام دهیم تا پلیمری بیرنگ و بیبو به دست آوریم.
چشمانداز آینده و چالشهای باقیمانده
ما اکنون در نقطهای ایستادهایم که پلیمریزاسیون رادیکالی کنترلشده با نور (Photo-CRP) از مرحله اثبات مفهوم در آزمایشگاه عبور کرده و به بلوغ تکنولوژیکی نزدیک میشود. با این حال، برای اینکه این روشها بتوانند جایگزین کامل سیستمهای حرارتی در مقیاس صنعتی شوند یا دریچههای جدیدی را در نانپزشکی باز کنند، ما باید بر محدودیتهای بنیادی فعلی غلبه کنیم. در این بخش پایانی، ما مرزهای دانش فعلی و مسیرهای نوظهور پژوهشی را که آینده این حوزه را شکل میدهند، ترسیم میکنیم.
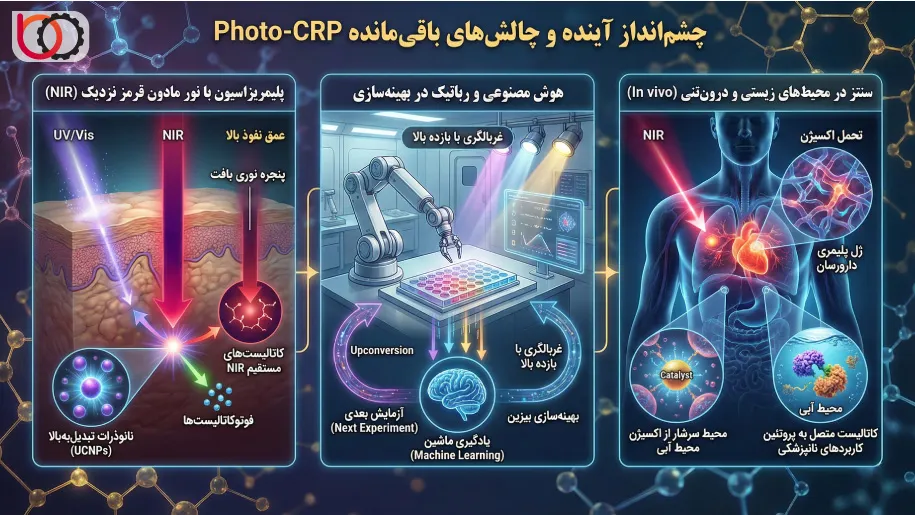
پلیمریزاسیون با نور مادون قرمز نزدیک (NIR): عبور از سد نفوذ
اکثر سیستمهای فوتوکاتالیستی که ما تا به امروز توسعه دادهایم، به نور فرابنفش (UV) یا مرئی (Vis) متکی هستند. اگرچه این طول موجها انرژی کافی برای انتقال الکترون را فراهم میکنند، اما ما با یک محدودیت فیزیکی جدی مواجه هستیم: عمق نفوذ کم. طبق قانون بیر-لامبرت، شدت نور با عبور از محیطهای کدر (مانند امولسیونها، کامپوزیتهای پرشده یا بافتهای بیولوژیکی) به صورت نمایی کاهش مییابد. این امر مقیاسپذیری و کاربردهای زیستی را محدود میکند.
ما برای حل این مشکل، تمرکز خود را به سمت «پنجره نوری بافت» یا ناحیه مادون قرمز نزدیک (NIR، طول موجهای ۷۰۰ تا ۱۰۰۰ نانومتر) معطوف کردهایم. فوتونهای NIR کمترین جذب و پراکندگی را در محیطهای آلی دارند. ما برای فعالسازی واکنشها با این فوتونهای کمانرژی، دو استراتژی پیچیده را دنبال میکنیم:
۱. استفاده از سیستمهای تبدیلبهبالا (Upconversion):
در این روش، ما از نانوذرات دوپشده با لانتانیدها (UCNPs) یا جفتهای رنگی آلی استفاده میکنیم که قادرند دو یا چند فوتون کمانرژی NIR را جذب کرده و یک فوتون پرانرژی (UV/Vis) ساطع کنند. این «آنتنهای نوری» در داخل محیط واکنش قرار میگیرند و به عنوان منابع نور داخلی عمل میکنند که کاتالیستهای معمولی را در اعماق بالا فعال میسازند.
۲. طراحی فوتوکاتالیستهای مستقیم NIR:
ما در حال سنتز کلاسهای جدیدی از رنگهای polymethine (مانند سیانینها) و کمپلکسهای فلزی (مانند باکتریوکلروفیلها) هستیم که مستقیماً قادر به جذب NIR و انجام انتقال الکترون هستند. چالش اصلی ما در اینجا، عمر کوتاه حالت برانگیخته در این رنگهاست که بازده واکنش را کاهش میدهد و نیازمند مهندسی دقیق مولکولی برای پایدارسازی ترازهای انرژی است.
ترکیب هوش مصنوعی و رباتیک در بهینهسازی Photo-CRP
فضای پارامترهای موثر بر یک واکنش پلیمریزاسیون نوری بسیار گسترده است: نوع کاتالیست، غلظت لیگاند، شدت نور، طول موج، حلال، دما و نوع مونومر. روش سنتی «آزمون و خطا» برای یافتن شرایط بهینه در این فضای چندبعدی، ناکارآمد و زمانبر است. ما اکنون شاهد ورود پارادایم «آزمایشگاههای خودران» (Self-Driving Labs) به شیمی پلیمر هستیم.
ما با ادغام رباتیک (برای انجام آزمایشهای اتوماتیک) و الگوریتمهای یادگیری ماشین (Machine Learning)، حلقههای بازخورد بستهای ایجاد میکنیم.
- غربالگری با بازده بالا (High-Throughput Screening): رباتها صدها واکنش را در مقیاس میکرولیتر و در شرایط نوری مختلف به صورت موازی انجام میدهند.
- بهینهسازی بیزین (Bayesian Optimization): الگوریتمهای هوش مصنوعی نتایج (مانند درصد تبدیل، $M_n$ و PDI) را تحلیل کرده و به جای جستجوی تصادفی، آزمایش بعدی را به گونهای پیشنهاد میدهند که بیشترین اطلاعات را فراهم کند یا به سمت هدف بهینه همگرا شود.
این رویکرد دادهمحور به ما اجازه میدهد تا کاتالیستهای جدید را با سرعتی غیرقابل مقایسه با روشهای انسانی کشف کنیم و شرایط واکنش را برای هر مونومر خاص دقیقاً تنظیم نماییم.
سنتز در محیطهای زیستی و درونتنی (In vivo)
نهایت آرزوی ما در Photo-CRP، توانایی انجام پلیمریزاسیون در داخل بدن موجودات زنده است. تصور کنید بتوانیم یک ژل پلیمری دارورسان را دقیقاً در محل تومور یا بافت آسیبدیده با تابش نور از بیرون بدن سنتز کنیم.
برای رسیدن به این هدف، ما باید بر چالشهای زیستسازگاری غلبه کنیم:
- تحمل اکسیژن: محیط سلولی سرشار از اکسیژن است و سیستمهای ما باید بدون نیاز به گاززدایی عمل کنند.
- پایداری در آب: بسیاری از کاتالیستهای فعلی در آب نامحلول هستند یا هیدرولیز میشوند. ما در حال توسعه کاتالیستهای متصل به پروتئین (Protein-conjugated catalysts) یا سیستمهای کپسوله شده هستیم که در فیزیولوژی بدن پایدار بمانند.
پروتکل اجرایی استاندارد و ملاحظات ایمنی در آزمایشگاه
ما تا این مرحله، مبانی تئوری و مکانیسمهای پیچیده را پوشش دادیم. اما برای تبدیل این دانش به یک پلیمر واقعی با شاخص پراکندگی (PDI) زیر ۱.۱، نیازمند رعایت دقیق جزئیات اجرایی هستیم. در این بخش، ما یک پروتکل استاندارد (SOP) را برای راهاندازی یک واکنش Photo-CRP ترسیم میکنیم که حاصل تجربیات عملی در آزمایشگاههای پیشرفته پلیمر است. عدم رعایت این ظرایف، اغلب دلیل اصلی شکست در تکرارپذیری نتایج است.
آمادهسازی پیشازواکنش: مدیریت نور و اتمسفر
نخستین اصلی که ما در آزمایشگاه رعایت میکنیم، حفاظت از محلولهای استوک در برابر نور محیط است. بسیاری از فوتوکاتالیستها (مانند ائوزین Y یا کمپلکسهای ایریدیم) حتی به نور فلورسنت سقف آزمایشگاه حساس هستند. ما همیشه از ظروف شیشهای کهربایی (Amber Glassware) استفاده میکنیم یا ویالها را با فویل آلومینیومی میپوشانیم.
در مرحله توزین و مخلوط کردن، اگر از سیستمهای «حساس به اکسیژن» استفاده میکنیم، تمام مراحل را در گلاو-باکس (Glovebox) یا با استفاده از تکنیکهای سرنگ (Schlenk Line) انجام میدهیم. حتی در سیستمهای دارای تحمل اکسیژن (Oxygen Tolerant)، ما توصیه میکنیم برای دستیابی به بالاترین وزن مولکولی و کمترین زمان القا، محلول واکنش را حداقل به مدت ۱۰ دقیقه با گاز نیتروژن یا آرگون خالصسازی (Purge) کنیم. وجود اکسیژن حلشده، هرچند واکنش را متوقف نمیکند، اما باعث مصرف کاتالیست و تولید محصولات جانبی اکسید شده میشود که در آنالیزهای دقیق (مانند MALDI-TOF) به صورت پیکهای مزاحم ظاهر میشوند.
هندسه ستاپ نوری و مدیریت دما
ما در چیدمان راکتور، فاصله منبع نور تا ویال واکنش را به عنوان یک متغیر بحرانی ثابت نگه میداریم (معمولاً ۲ تا ۵ سانتیمتر). تغییر اندک در این فاصله، طبق قانون عکس مجذور فاصله، شدت نور فرودی را به شدت تغییر میدهد و سینتیک واکنش را غیرقابل مقایسه میکند.
حرارت تولید شده توسط منابع نوری (بهویژه LEDهای توان بالا) دشمن کنترل وزن مولکولی است. اگر دما افزایش یابد، سرعت انتشار ($k_p$) و سرعت اختتام ($k_t$) با نرخهای متفاوتی تغییر میکنند و ممکن است کنترل واکنش از دست برود. ما همیشه از یک حمام آب گردشی (Circulating Water Bath) یا یک فن قوی جهت خنکسازی ویال واکنش استفاده میکنیم تا دما را در محدوده $\pm ۱$ درجه سانتیگراد ثابت نگه داریم. در گزارشدهی نتایج، ذکر دقیق دمای داخلی محلول (نه دمای اتاق) برای تکرارپذیری الزامی است.
پایش واکنش (Monitoring) و نمونهبرداری
ما برای رسم نمودارهای سینتیکی دقیق، نیاز به برداشت نمونه در فواصل زمانی مشخص داریم. در سیستمهای Photo-CRP، قطع و وصل نور برای نمونهبرداری میتواند باعث توقف موقت واکنش شود. برای به حداقل رساندن این اثر، ما از سرنگهای ضد-نور یا سوزنهای بلند استفاده میکنیم و نمونهبرداری را در سریعترین زمان ممکن انجام میدهیم.
هر نمونه برداشته شده باید بلافاصله «کویینچ» (Quench) شود. ما معمولاً نمونه را در معرض هوا قرار میدهیم و به آن حلال سرد حاوی بازدارنده رادیکال (مانند MEHQ) اضافه میکنیم. سپس نمونهها برای آنالیز رزونانس مغناطیسی هسته ($^1H-NMR$) جهت تعیین درصد تبدیل و کروماتوگرافی ژلتراوا (GPC/SEC) جهت تعیین وزن مولکولی ارسال میشوند.
ایمنی و بهداشت حرفهای (HSE)
کار با منابع نوری پرقدرت خطرات منحصربهفردی دارد که ما باید جدی بگیریم:
۱. خطر اشعه UV و نور آبی: تابش مستقیم یا بازتابی نورهای UV و آبی پرقدرت میتواند آسیبهای جبرانناپذیری به شبکیه چشم و پوست وارد کند. ما استفاده از عینکهای محافظ مخصوص (با فیلتر طول موج مربوطه) و محفظههای واکنش پوشیده (Black Box) را الزامی میدانیم.
۲. سمیت کاتالیستها و مونومرها: بسیاری از مونومرهای اککریلاتی و فوتوکاتالیستهای آلی، حساسیتزا یا سمی هستند. تمام مراحل آمادهسازی باید زیر هود شیمیایی با تهویه مناسب انجام شود.
۳. خطر انفجار: در مقیاسهای بزرگ، پلیمریزاسیون میتواند بسیار گرمازا (Exothermic) باشد. ترکیب گرمای واکنش با گرمای منبع نور ممکن است منجر به افزایش فشار و شکستن ظروف شیشهای شود. استفاده از شیلدهای محافظ صورت همواره توصیه میشود.
پرسشهای متداول تخصصی (FAQ)
ما در انتهای این مقاله جامع، به برخی از پرتکرارترین و فنیترین سوالاتی که پژوهشگران و مهندسان پلیمر در هنگام کار با سیستمهای Photo-CRP با آنها مواجه میشوند، پاسخ میدهیم. این بخش برای رفع ابهامات سریع و عیبیابی (Troubleshooting) طراحی شده است.
۱. تفاوت اصلی بین مکانیسم Photo-ATRP و Photo-RAFT در چیست؟
تفاوت بنیادین در نحوه کنترل انتهای زنجیر است. در Photo-ATRP، ما با یک تعادل دینامیک اکسیداسیون-احیاء (Redox) سروکار داریم که در آن یک هالوژن (معمولاً برم یا کلر) بین زنجیر پلیمر و کاتالیست فلزی/آلی جابجا میشود. اما در Photo-RAFT، مکانیسم بر پایه انتقال زنجیر تباهیده (Degenerative Chain Transfer) استوار است که در آن یک گروه تیوکربنیل (S=C-S) بین زنجیرهای فعال و غیرفعال مبادله میشود. Photo-ATRP بیشتر به سینتیک انتقال الکترون وابسته است، در حالی که Photo-RAFT به پایداری رادیکال میانی وابسته است.
۲. آیا میتوانیم از هر نوع منبع نوری برای این واکنشها استفاده کنیم؟
خیر. تطبیق طیفی (Spectral Overlap) حیاتی است. طیف نشر لامپ (Emission Spectrum) باید دقیقاً با طیف جذب (Absorption Spectrum) فوتوکاتالیست همپوشانی داشته باشد. برای مثال، اگر کاتالیست ائوزین Y (جذب ماکزیمم در ~۵۳۰ نانومتر) استفاده میکنید، باید از LED سبز استفاده کنید. استفاده از نور سفید یا UV برای کاتالیستهای مرئی ممکن است باعث تخریب کاتالیست یا واکنشهای جانبی ناخواسته شود. همچنین شدت نور ($mW/cm^2$) باید کافی باشد تا سرعت تولید رادیکال بر سرعت اختتام غلبه کند.
۳. چرا پلیمریزاسیون من پس از چند دقیقه متوقف میشود (Dead Polymerization)؟
این مشکل معمولاً به دو دلیل رخ میدهد:
۱. تخریب کاتالیست (Photobleaching): شدت نور بیش از حد زیاد بوده و ساختار کاتالیست را تخریب کرده است.
۲. تجمع اکسیژن: اگر سیستم کاملاً نسبت به هوا ایزوله نباشد یا سرعت نفوذ اکسیژن بیشتر از سرعت مصرف آن توسط کاتالیست باشد، رادیکالهای پروکسی تشکیل شده و واکنش متوقف میشود. بررسی مجدد گاززدایی و کاهش شدت نور پیشنهاد میشود.
۴. چگونه میتوانم کاتالیست فلزی (مثلاً مس) را به طور کامل از محصول نهایی حذف کنم؟
حتی در مقادیر ppm، مس میتواند باعث رنگی شدن پلیمر شود. روشهای استاندارد ما عبارتند از:
عبور محلول پلیمر از ستون آلومینا (Alumina Column) یا سیلیکا ژل.
استفاده از رزینهای تبادل یونی (Ion Exchange Resins).
رسوبدهی مجدد (Reprecipitation) پلیمر در حلال سرد (مانند متانول یا هگزان).
استفاده از لیگاندهای جامد یا ساپورتشده که کاتالیست را در فاز ناهمگن نگه میدارند.
۵. آیا سیستمهای Photo-CRP برای سنتز پلیمرهای زیستی (Bio-polymers) مناسب هستند؟
بله، به شرط انتخاب شرایط صحیح. سیستمهای Photo-RAFT و O-ATRP (بدون فلز) که تحت نور مرئی (Visible Light) و در محیط آبی (Aqueous Media) کار میکنند، بهترین گزینهها هستند. نور مرئی انرژی کافی برای تخریب پروتئینها یا DNA را ندارد و دمای اتاق نیز شرایط فیزیولوژیک را حفظ میکند. با این حال، باید از کاتالیستهای سمی و حلالهای آلی اجتناب شود.