پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (پلیمریزاسیون NMP)
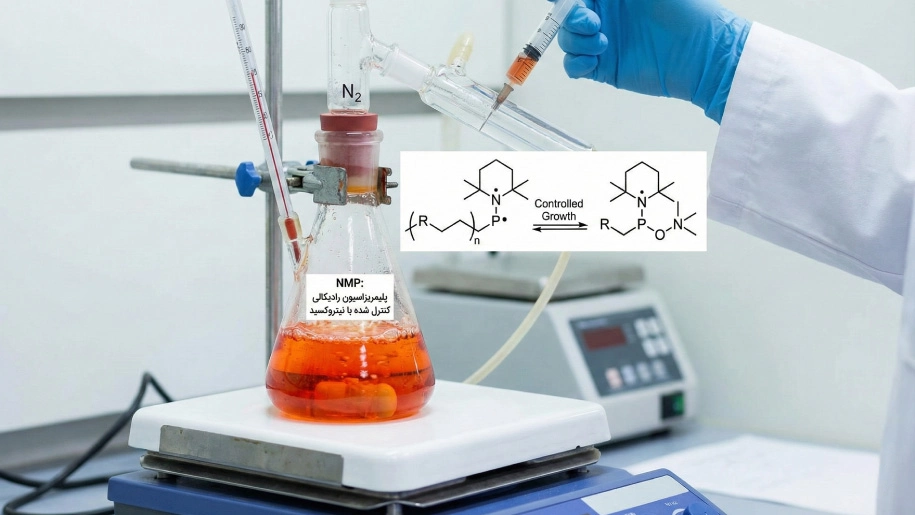
پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید یا همان پلیمریزاسیون NMP که در متون علمی با نام SFRP (پلیمریزاسیون رادیکالی پایدار) نیز شناخته میشود، یکی از روشهای اصلی در خانواده پلیمریزاسیون رادیکالی غیرفعالسازی برگشتپذیر (RDRP) است. این تکنیک برای اولین بار در دهه ۱۹۹۰ توسعه یافت و هدف اصلی آن، غلبه بر محدودیتهای ذاتی «پلیمریزاسیون رادیکالی آزاد» (FRP)، یعنی عدم کنترل بر وزن مولکولی و توزیع آن بود.
در فرآیندهای سنتی رادیکالی، واکنشهای اختتام (Termination) به سرعت رخ میدهند و منجر به تولید زنجیرهای مرده با طولهای نابرابر میشوند. اما در فرآیند NMP، با استفاده از یک رادیکال پایدار نیتروکسیدی (مانند TEMPO یا SG1)، انتهای زنجیرهای پلیمری به صورت برگشتپذیر غیرفعال میشود. این مکانیزم به شیمیدانان اجازه میدهد تا پلیمرهایی با شاخص پراکندگی (PDI) بسیار پایین (معمولاً بین ۱.۱ تا ۱.۳)، وزن مولکولی قابل پیشبینی و معماریهای پیچیده (مانند کوپلیمرهای قطعهای) سنتز کنند.
مزیت رقابتی پلیمریزاسیون NMP نسبت به روشهای رقیب مانند ATRP (پلیمریزاسیون رادیکالی انتقال اتم)، عدم نیاز به کاتالیزورهای فلزی (مانند مس) و لیگاندهای سمی است. سیستم NMP تنها بر پایه «تعادل حرارتی» عمل میکند؛ به این معنی که فرآیند پلیمریزاسیون صرفاً با افزایش دما فعال شده و با کاهش آن متوقف میشود. این ویژگی، NMP را به گزینهای ایدهآل برای تولید پلیمرهای گرید الکترونیک و بیومتریال که نیازمند خلوص بالا و عدم آلودگی فلزی هستند، تبدیل کرده است.
- مکانیسم پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP) و تعادلات شیمیایی
- پدیده اثر رادیکال پایدار (PRE) در فرآیند NMP
- آغازگرهای دومولکولی در سیستم NMP؛ استفاده از BPO و TEMPO
- سنتز و کاربرد آلکوکسی آمین ها به عنوان آغازگر تکمولکولی NMP
- سنتز و کاربرد آلکوکسی آمین ها به عنوان آغازگر تکمولکولی NMP
- کاربرد رادیکال TEMPO در پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید
- رادیکالهای SG1 و TIPNO؛ نسل جدید نیتروکسید برای آکریلاتها
- سینتیک پلیمریزاسیون NMP؛ محاسبه ثابت سرعت و شاخص پراکندگی (PDI)
- انواع مونومرهای قابل استفاده در NMP و مشکل متاکریلاتها
- واکنشهای جانبی مخرب در فرآیند NMP
- تاثیر حلال و دما بر سرعت پلیمریزاسیون NMP
- مقایسه پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP) با ATRP و RAFT
- سنتز کوپلیمرهای قطعهای (Block Copolymers) با روش NMP
- ساخت پلیمرهای ستارهای و شاخهدار با تکنیک NMP
- کاربردهای صنعتی پلیمرهای سنتز شده با NMP
- روشهای آنالیز پلیمر NMP؛ طیفسنجی ESR و کروماتوگرافی GPC
- آینده تکنولوژی NMP؛ روشهای نوری و دمای محیط
- نتیجه گیری
مکانیسم پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP) و تعادلات شیمیایی
اساس مکانیسم پلیمریزاسیون NMP بر پایه یک تعادل برگشتپذیر حرارتی بین گونههای «فعال» (Active) و «غیرفعال» (Dormant) استوار است. برخلاف پلیمریزاسیون رادیکالی آزاد که در آن رادیکالها دائماً فعال هستند و به سرعت با هم ترکیب میشوند، در NMP، انتهای زنجیر در بیشتر زمان واکنش توسط یک گروه محافظ (نیتروکسید) پوشانده شده است.
معادله کلی تعادل در این فرآیند به صورت زیر نمایش داده میشود:
$$P-ON <\underset{k_{deact}}{\overset{k_{act}}{\rightleftharpoons}}> P^\bullet + ^\bullet ON$$
در این معادله:
- $P-ON$: گونه غیرفعال یا همان ماکروآلکوکسیآمین (Macroalkoxyamine) است.
- $P^\bullet$: رادیکال پلیمری در حال رشد (Propagating Radical) است که توانایی اضافه کردن مونومر را دارد.
- $^\bullet ON$: رادیکال پایدار نیتروکسید (مانند TEMPO) است که به عنوان عامل کنترلکننده (Mediator) عمل میکند.
- $k_{act}$ و $k_{deact}$: به ترتیب ثابتهای سرعت فعالسازی (Activation) و غیرفعالسازی (Deactivation) هستند.
نقش تعادل برگشتپذیر همولیز (Reversible Homolysis) در کنترل واکنش
کلید موفقیت در پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP)، پایین نگه داشتن غلظت لحظهای رادیکالهای فعال ($[P^\bullet]$) است. طی فرآیند «همولیز برگشتپذیر»، پیوند کووالانسی کربن-اکسیژن ($C-O$) در گونه غیرفعال میشکند و رادیکال فعال برای مدت زمان بسیار کوتاهی آزاد میشود.
در این بازه زمانی کوتاه، رادیکال $P^\bullet$ با تعدادی مولکول مونومر واکنش میدهد (زنجیر رشد میکند). بلافاصله پس از آن، رادیکال پایدار نیتروکسید ($^\bullet ON$) با رادیکال فعال برخورد کرده و مجدداً گونه غیرفعال را تشکیل میدهد (Recombination).
این چرخه مداوم فعالسازی و غیرفعالسازی باعث میشود که احتمال برخورد دو زنجیر پلیمری فعال با یکدیگر (Termination) به شدت کاهش یابد. به بیان دقیقتر، تعادل واکنش به شدت به سمت گونههای غیرفعال متمایل است ($K_{eq} \ll 1$)، به طوری که در هر لحظه، تنها بخش بسیار ناچیزی (در حد $10^{-8}$ مول بر لیتر) از زنجیرها فعال هستند.
تاثیر دما بر ثابت سرعت فعالسازی ($k_{act}$) و شکست پیوند C-O
از آنجا که شکستن پیوند $C-O$ یک فرآیند گرماگیر است، مکانیسم پلیمریزاسیون NMP وابستگی شدیدی به دما دارد. انرژی فعالسازی ($E_a$) برای همولیز این پیوند در آغازگرهای متداول نیتروکسیدی، معمولاً بین ۱۱۰ تا ۱۳۰ کیلوژول بر مول است.
افزایش دما باعث افزایش نمایی ثابت سرعت فعالسازی ($k_{act}$) طبق رابطه آرنیوس میشود. بنابراین، کنترل دما در راکتور حیاتی است:
- دمای پایین: انرژی کافی برای شکست پیوند وجود ندارد و واکنش متوقف میشود (حالت فریز).
- دمای بهینه: سرعت تولید رادیکالهای فعال به اندازهای است که پلیمریزاسیون با سرعت معقول پیش رود، اما غلظت رادیکالها آنقدر بالا نمیرود که واکنشهای جانبی و اختتام برگشتناپذیر غالب شوند.
برای مثال، در سیستمهای مبتنی بر TEMPO برای استایرن، دما باید بالای ۱۲۰ درجه سانتیگراد باشد تا تعادل به سمت راست جابجا شود، در حالی که در سیستمهای نسل جدید مانند SG1، به دلیل ضعف پیوند $C-O$، واکنش در دماهای پایینتر (حدود ۹۰ درجه) امکانپذیر است.
پدیده اثر رادیکال پایدار (PRE) در فرآیند NMP
موفقیت سیستمهای پلیمریزاسیون NMP در کنترل وزن مولکولی، مدیون یک پدیده سینتیکی خودکار به نام اثر رادیکال پایدار (Persistent Radical Effect – PRE) است. این پدیده توضیح میدهد که چرا در حضور یک رادیکال پایدار (مانند نیتروکسید) که تمایلی به واکنش با خودش ندارد، واکنشهای اختتام بین رادیکالهای فعال (Transient Radicals) به شدت سرکوب میشوند.
در واقع، اثر رادیکال پایدار (PRE) یک اصل عمومی در شیمی رادیکالی است که تضمین میکند تعادل واکنش به نفع گونههای غیرفعال (Dormant) باقی بماند و واکنش «فرار» (Runaway) نکند.
قانون فیشر (Fischer’s Law) و تجمع رادیکالهای نیتروکسید
هانس فیشر (H. Fischer) در سال ۱۹۸۶ مدل ریاضی دقیقی برای این پدیده ارائه کرد. طبق قانون فیشر، در لحظات اولیه شروع واکنش، مقدار اندکی از رادیکالهای پلیمری فعال ($P^\bullet$) با یکدیگر واکنش داده و از بین میروند (Termination). از آنجا که رادیکالهای نیتروکسید ($^\bullet ON$) با یکدیگر واکنش نمیدهند (Dimerization ندارند)، غلظت آنها در محیط واکنش به تدریج افزایش مییابد.
این تجمعِ اضافیِ رادیکالهای پایدار، طبق اصل لوشاتلیه، تعادل را به سمت چپ (تشکیل گونههای غیرفعال $P-ON$) هل میدهد. رابطه تحلیلی فیشر نشان میدهد که حاصلضرب غلظت رادیکالهای فعال و پایدار در طول زمان ثابت میماند:
$$[P^\bullet] \cdot [^\bullet ON] = K_{eq} \cdot [P-ON]$$
با افزایش غلظت $[^\bullet ON]$، غلظت $[P^\bullet]$ باید کاهش یابد. این مکانیزم خودتنظیمی باعث میشود که غلظت رادیکالهای فعال به سطحی بسیار پایین (در حد ppb) برسد که عملاً احتمال برخورد دو رادیکال فعال را به صفر میل میدهد.
نحوه سرکوب واکنشهای اختتام (Termination) توسط رادیکالهای پایدار
در یک سیستم پلیمریزاسیون ایدهآل، هدف ما حذف کامل واکنشهای پایان (Termination) است. در فرآیند NMP، حضور مازاد رادیکالهای پایدار باعث میشود که سرعت واکنش «غیرفعالسازی» (Deactivation) بسیار بیشتر از سرعت واکنش «اختتام» شود.
اگر سرعت غیرفعالسازی را $R_{deact}$ و سرعت اختتام را $R_t$ در نظر بگیریم، نسبت آنها به صورت زیر است:
$$\frac{R_{deact}}{R_t} = \frac{k_{deact}[P^\bullet][^\bullet ON]}{2k_t[P^\bullet]^2} = \frac{k_{deact}[^\bullet ON]}{2k_t[P^\bullet]}$$
با توجه به اینکه طبق بخش قبل، غلظت $[^\bullet ON]$ بسیار بیشتر از $[P^\bullet]$ است، صورت کسر بسیار بزرگتر از مخرج میشود.
این یعنی هرگاه یک رادیکال پلیمری ($P^\bullet$) تشکیل شود، احتمال برخورد آن با یک رادیکال نیتروکسید و بازگشت به حالت خوابیده ($P-ON$)، هزاران برابر بیشتر از احتمال برخورد با یک رادیکال پلیمری دیگر و مرگ زنجیر است. این مکانیسم دقیقی است که باعث میشود زنجیرها «زنده» بمانند و با سرعتی برابر رشد کنند.
آغازگرهای دومولکولی در سیستم NMP؛ استفاده از BPO و TEMPO
در تاریخچه توسعه پلیمریزاسیون NMP، اولین رویکرد عملی استفاده از سیستمهای «دومولکولی» (Bimolecular Systems) بود. در این روش، آغازگر پلیمریزاسیون و عامل کنترلکننده (نیتروکسید) به عنوان دو ترکیب مجزا به راکتور اضافه میشوند. این روش به دلیل در دسترس بودن مواد اولیه تجاری، همچنان در برخی فرآیندهای صنعتی ارزانقیمت استفاده میشود.
سیستم سنتی بنزوئیل پراکسید (BPO) و رادیکال تمپو (TEMPO)
در یک سیستم کلاسیک دومولکولی، ما از یک آغازگر حرارتی متداول (مانند بنزوئیل پراکسید یا BPO) برای تولید رادیکالهای اولیه و از یک رادیکال پایدار آزاد (مانند TEMPO) برای به دام انداختن آنها استفاده میکنیم.
مکانیسم شروع واکنش به صورت «درجا» (In-situ) انجام میشود:
- آغازگر حرارتی تجزیه شده و رادیکالهای آزاد ($I^\bullet$) تولید میکند.
- این رادیکالها به اولین مولکول مونومر حمله کرده و زنجیر کوتاه در حال رشد را میسازند.
- سپس، رادیکال TEMPO موجود در محیط، با این زنجیر جفت شده و اولین گونه غیرفعال (Alkoxyamine) را درون راکتور میسازد.
این روش برای پلیمریزاسیون استایرن در دمای ۱۲۵ تا ۱۳۵ درجه سانتیگراد بسیار متداول است.
مشکلات کنترل نسبت مولی و راندمان شروع در سیستمهای دوجزیی
چالش مهندسی اصلی در سیستم NMP دومولکولی، تنظیم دقیق «استوکیومتری» است. برای کنترل ایدهآل، نسبت غلظت رادیکالهای فعال به رادیکالهای نیتروکسید باید دقیق باشد.
- مشکل راندمان آغازگر ($f < 1$): تمام مولکولهای BPO لزوماً زنجیر پلیمری را شروع نمیکنند (برخی در اثر واکنشهای جانبی “Cage Effect” از بین میروند). بنابراین، اگر نسبت مولی BPO به TEMPO را دقیقاً ۱:۱ بگیریم، در عمل تعداد رادیکالهای TEMPO بیشتر از رادیکالهای فعال خواهد شد.
- دوره القا (Induction Period): مازاد بودن TEMPO در ابتدای واکنش باعث میشود که تمام رادیکالهای فعال بلافاصله شکار شوند و سرعت واکنش در ساعات اولیه بسیار کند باشد.
- عدم کنترل: اگر مقدار TEMPO کمتر از حد نیاز باشد، واکنش از کنترل خارج شده و به سمت پلیمریزاسیون رادیکالی آزاد (FRP) میل میکند.
سنتز و کاربرد آلکوکسی آمین ها به عنوان آغازگر تکمولکولی NMP
برای حل مشکلات استوکیومتری سیستمهای دومولکولی، شیمیدانان به سمت استفاده از «آغازگرهای تکمولکولی» (Unimolecular Initiators) حرکت کردند. در این روش، گونه غیرفعال ($R-ON$) از قبل در آزمایشگاه سنتز و خالصسازی شده و سپس به عنوان یک پودر یا مایع خالص به راکتور اضافه میشود. به این ترکیبات پیشساخته، آلکوکسی آمین میگویند.
روشهای سنتز آلکوکسی آمینهای یونیمولکولار برای شروع دقیق
استفاده از آلکوکسی آمینها در فرآیند NMP تضمین میکند که نسبت رادیکال آغازگر ($R^\bullet$) و عامل کنترلکننده ($^\bullet ON$) دقیقاً ۱ به ۱ است.
هنگامی که این مولکول حرارت میبیند، پیوند $C-O$ شکسته شده و همزمان یک رادیکال فعال (برای شروع زنجیر) و یک رادیکال نیتروکسید (برای کنترل زنجیر) آزاد میشود.
این روش مزایای صنعتی مشخصی دارد:
- حذف دوره القا: واکنش بلافاصله پس از رسیدن به دمای هدف آغاز میشود.
- کنترل ساختار: با انتخاب ساختار بخش $R$ در آلکوکسی آمین، میتوان گروههای عاملی خاصی را دقیقاً در ابتدای زنجیر پلیمری قرار داد (End-group fidelity).
مقایسه پایداری حرارتی و دمای تفکیک آغازگرهای مختلف
عملکرد یک آغازگر تکمولکولی مستقیماً به انرژی پیوند $C-O$ در ساختار آن وابسته است. این انرژی تعیین میکند که پلیمریزاسیون در چه دمایی انجام شود:
- آلکوکسی آمینهای بر پایه TEMPO: پیوند بسیار قوی دارند و برای فعالسازی نیاز به دمای بالای ۱۲۵ درجه سانتیگراد دارند. این دما برای بسیاری از مونومرهای حساس مناسب نیست.
- آلکوکسی آمینهای نسل جدید (پایه SG1): با تغییر ساختار شیمیایی و ایجاد ممانعت فضایی روی نیترژن، پیوند $C-O$ تضعیف شده است. این ترکیبات در دماهای پایینتر (بین ۸۰ تا ۱۰۰ درجه) تفکیک میشوند که اجازه میدهد طیف وسیعتری از مونومرها (مانند آکریلاتها) با سرعت مناسب پلیمریزه شوند.
سنتز و کاربرد آلکوکسی آمین ها به عنوان آغازگر تکمولکولی NMP
برای غلبه بر عدم قطعیتهای استوکیومتری در سیستمهای دومولکولی، پارادایم شیمی سنتز به سمت توسعه «آغازگرهای تکمولکولی» (Unimolecular Initiators) حرکت کرده است. در این روش، گونه غیرفعال ($R-ON$) که در سیستمهای سنتی در حین واکنش تشکیل میشد، قبلاً در آزمایشگاه سنتز و خالصسازی شده و تحت نام عمومی آلکوکسی آمین به راکتور اضافه میشود. این ترکیبات، نقش دوگانه آغازگر و کنترلکننده را در قالب یک مولکول واحد ایفا میکنند.
روشهای سنتز آلکوکسی آمینهای یونیمولکولار برای شروع دقیق
استفاده از آغازگر تکمولکولی در سیستم NMP، یک مزیت ترمودینامیکی و مهندسی قاطع ایجاد میکند: تضمین نسبت دقیق ۱ به ۱ میان رادیکالهای فعال ($P^\bullet$) و رادیکالهای نیتروکسید ($^\bullet ON$).
هنگامی که آلکوکسی آمین حرارت میبیند، پیوند کووالانسی حساس $C-O$ شکسته شده و همزمان یک رادیکال برای شروع زنجیر و یک رادیکال برای کنترل آن آزاد میشود.
مزایای فنی این روش در مقیاس صنعتی عبارتند از:
- حذف دوره القا: برخلاف سیستمهای دوجزیی که نیاز به زمان برای تعادلسازی دارند، در اینجا واکنش بلافاصله پس از رسیدن به دمای انحلال آغاز میشود.
- کنترل ساختار (End-group Fidelity): با مهندسی شیمیایی بخش $R$ در ساختار آلکوکسی آمین، میتوان گروههای عاملی خاص (مانند هیدروکسیل یا کربوکسیل) را دقیقاً در ابتدای زنجیر پلیمری قرار داد. این ویژگی برای سنتز پلیمرهای تلهکیم (Telechelic) ضروری است.
- دقت وزن مولکولی: از آنجا که تعداد دقیق مولکولهای آغازگر مشخص است، وزن مولکولی هدف ($M_n$) صرفاً تابعی از نسبت غلظت مونومر به غلظت آلکوکسی آمین خواهد بود:$$M_n = \text{Conversion} \times \frac{[M]_0}{[\text{Alkoxyamine}]_0} \times MW_{monomer}$$
مقایسه پایداری حرارتی و دمای تفکیک آغازگرهای مختلف
عملکرد سینتیکی یک آلکوکسی آمین، مستقیماً به انرژی پیوند اکسیژن-کربن در ساختار آن وابسته است. این انرژی تعیین میکند که واکنش پلیمریزاسیون در چه دمایی فعال شود. شیمیدانان با تغییر گروههای جانبی روی نیتروژن، پایداری این پیوند را دستکاری میکنند:
- آغازگرهای نسل اول (TEMPO-based): پیوند $C-O$ در این ترکیبات بسیار پایدار است. برای غلبه بر انرژی فعالسازی و شکستن پیوند، به دماهای بالای ۱۲۵ درجه سانتیگراد نیاز است. این دمای بالا استفاده از آنها را برای مونومرهای با نقطه جوش پایین محدود میکند.
- آغازگرهای نسل جدید (SG1/TIPNO-based): در این ساختارها، با افزودن گروههای حجیم فضایی (Steric Hindrance) یا گروههای الکترونکشنده، پیوند $C-O$ تضعیف شده است. این امر باعث میشود که آلکوکسی آمین در دماهای پایینتر (بین ۸۰ تا ۱۰۰ درجه سانتیگراد) تفکیک شود. کاهش دمای عملیاتی، امکان پلیمریزاسیون کنترلشده طیف وسیعتری از مونومرها (از جمله آکریلاتها و آکریلآمیدها) را با سرعت مناسب فراهم میکند.
کاربرد رادیکال TEMPO در پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید
در تاریخچه توسعه پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP)، مولکول TEMPO (۲،۲،۶،۶-تترامتیل پیپریدینیل-۱-اکسی) جایگاه ویژهای دارد. این ترکیب نخستین رادیکال پایداری بود که توانایی کنترل زنده واکنشهای پلیمریزاسیون را اثبات کرد و همچنان به عنوان استانداردی برای مقایسه عملکرد سایر نیتروکسیدها شناخته میشود. اگرچه نسلهای جدیدتر معرفی شدهاند، اما TEMPO همچنان برای تولید پلیاستایرن با توزیع وزن مولکولی باریک در مقیاس صنعتی استفاده میشود.
ساختار شیمیایی TEMPO و محدودیت فضایی آن
پایداری فوقالعاده رادیکال TEMPO ناشی از ساختار شیمیایی منحصربهفرد آن است. در این مولکول، الکترون جفتنشده روی اتم اکسیژن قرار دارد که توسط چهار گروه متیل حجیم روی کربنهای آلفا (موقعیتهای ۲ و ۶ حلقه پیپریدین) احاطه شده است.
این گروههای متیل، یک «ممانعت فضایی» (Steric Hindrance) شدید ایجاد میکنند. این ممانعت دو اثر حیاتی دارد:
- جلوگیری از دیمریزاسیون: TEMPO برخلاف رادیکالهای کربنی معمولی، نمیتواند با یک مولکول TEMPO دیگر واکنش دهد. این ویژگی اساس «اثر رادیکال پایدار» است.
- انتخابگری در واکنش: TEMPO تنها میتواند با رادیکالهای فعال پلیمری (که معمولاً ممانعت فضایی کمتری دارند) واکنش دهد و پیوند ضعیف $C-O$ را تشکیل دهد.
با این حال، همین ممانعت فضایی باعث میشود که TEMPO در شکار رادیکالهای بسیار حجیم یا واکنش در دماهای پایین، کُند عمل کند.
چرا TEMPO فقط برای استایرن و در دمای بالا (۱۲۵ درجه) کارایی دارد؟
علیرغم موفقیت در آزمایشگاه، کاربرد صنعتی رادیکال TEMPO عمدتاً محدود به پلیمریزاسیون استایرن و مشتقات آن است. این محدودیت دو دلیل عمده ترمودینامیکی و سینتیکی دارد:
- انرژی پیوند C-O: پیوند تشکیل شده بین TEMPO و انتهای زنجیر پلیاستایرن، پایداری حرارتی نسبتاً بالایی دارد. برای اینکه سرعت شکست این پیوند ($k_{act}$) به حد مطلوب برای پیشرفت واکنش برسد، دمای راکتور باید به بالای ۱۲۵ تا ۱۳۵ درجه سانتیگراد افزایش یابد. در دماهای پایینتر، زنجیرها در حالت «خوابیده» باقی میمانند و واکنشی رخ نمیدهد.
- ضریب تعادل ($K$): برای مونومرهایی مانند آکریلاتها، پیوند TEMPO-Polymer بیش از حد قوی است (ضریب تعادل $K$ بسیار کوچک است). این باعث میشود که سرعت پلیمریزاسیون بسیار کُند باشد. تلاش برای افزایش دما جهت تسریع واکنش آکریلاتها نیز بیفایده است، زیرا در دماهای بالا واکنشهای جانبی مخرب غالب میشوند.
- خودشروعی حرارتی استایرن: استایرن در دمای ۱۲۵ درجه سانتیگراد به صورت خودبهخودی (Thermal Self-initiation) رادیکال آزاد تولید میکند. این ویژگی به جبران رادیکالهای از دست رفته در طول واکنش کمک کرده و سینتیک TEMPO را پایدار نگه میدارد؛ مزیتی که سایر مونومرها فاقد آن هستند.
رادیکالهای SG1 و TIPNO؛ نسل جدید نیتروکسید برای آکریلاتها
محدودیتهای ساختاری TEMPO در کنترل پلیمریزاسیون مونومرهای غیر استایرنی، منجر به توسعه نسل دوم و سوم میانجیهای نیتروکسیدی شد. در این میان، رادیکال SG1 (که تجارتاً با نام BlocBuilder شناخته میشود) و TIPNO به عنوان موفقترین جایگزینهای صنعتی ظهور کردند. هدف اصلی طراحی این مولکولها، تضعیف انرژی پیوند $C-O$ به منظور امکانپذیر ساختن پلیمریزاسیون آکریلات و کاهش دمای واکنش بود.
معرفی نیتروکسیدهای آسیلیک (Acyclic) برای کاهش دمای واکنش
تفاوت بنیادین شیمیایی میان TEMPO و نسل جدید، در توپولوژی مولکولی است. در حالی که TEMPO یک ساختار حلقوی (Cyclic) صلب دارد، SG1 یک نیتروکسید آسیلیک (Acyclic) یا غیرحلقوی است که دارای یک گروه فسفونات در موقعیت بتا نسبت به نیتروژن میباشد.
این ساختار غیرحلقوی و وجود گروههای حجیم (مانند ترشیو-بوتیل)، ممانعت فضایی را افزایش داده و پایداری ترمودینامیکی رادیکال را تغییر میدهد. نتیجه این تغییر ساختار، افزایش قابل توجه در «ثابت سرعت تفکیک» ($k_d$) است.
به زبان سینتیکی، پیوند کووالانسی تشکیل شده بین SG1 و انتهای زنجیر پلیمر، سستتر از پیوند TEMPO است. این ویژگی اجازه میدهد تا همولیز در دماهای بسیار پایینتر (حدود ۹۰ تا ۱۱۰ درجه سانتیگراد) با سرعت کافی رخ دهد. کاهش دما نه تنها مصرف انرژی فرآیند را کاهش میدهد، بلکه از وقوع واکنشهای جانبی تخریبی در دماهای بالا جلوگیری میکند.
کنترل پلیمریزاسیون آکریلاتها و غلبه بر مشکلات نسل اول
مهمترین دستاورد فنی استفاده از رادیکال SG1 و همتایان آن، توانایی کنترل واکنش مونومرهای خانواده آکریلات (مانند بوتیل آکریلات و اتیل آکریلات) است.
در سیستمهای قدیمی مبتنی بر TEMPO، آکریلاتها یا اصلاً پلیمریزه نمیشدند یا واکنشی بسیار کُند و کنترلنشده داشتند. دلیل این امر، اتصال بیش از حد قوی TEMPO به رادیکال پلیآکریلات بود که مانع از رشد زنجیر میشد.
اما با استفاده از نیتروکسیدهای آسیلیک، ضریب تعادل ($K$) برای آکریلاتها بهینه شده است. این سیستمها امکان تولید پلیآکریلاتهایی با:
- وزن مولکولی بالا
- تبدیل (Conversion) بالا در زمان معقول
- شاخص پراکندگی (PDI) پایین (زیر ۱.۱۵) را فراهم میکنند. این پیشرفت، مسیر را برای سنتز صنعتی کوپلیمرهای قطعهای الاستومری (مانند پلیاستایرن-بلاک-پلیبوتیل آکریلات) بدون نیاز به کاتالیزورهای فلزی هموار کرد.
سینتیک پلیمریزاسیون NMP؛ محاسبه ثابت سرعت و شاخص پراکندگی (PDI)
بررسی رفتار سینتیک پلیمریزاسیون NMP در مقیاس آزمایشگاهی و صنعتی، تنها راه معتبر برای اثبات «زنده بودن» (Livingness) فرآیند است. برخلاف پلیمریزاسیون رادیکالی آزاد که در آن وزن مولکولی در همان ثانیههای اول به اوج میرسد و سپس ثابت میماند، در سیستم NMP پارامترهای مولکولی تابع زمان و میزان پیشرفت واکنش هستند. مهندسین پلیمر با رسم نمودارهای سینتیکی، صحت عملکرد آغازگر و عدم وجود واکنشهای جانبی را پایش میکنند.
بررسی رابطه خطی تبدیل و وزن مولکولی ($M_n$ vs Conversion)
اولین و مهمترین معیار برای کنترل کیفی فرآیند NMP، وجود یک رابطه خطی میان «درصد تبدیل مونومر» (Conversion) و «وزن مولکولی متوسط عددی» ($M_n$) است.
در یک سیستم ایدهآل، تمام زنجیرها همزمان شروع به رشد میکنند و با سرعت یکسانی بلند میشوند. بنابراین، وزن مولکولی باید دقیقاً متناسب با میزان مصرف مونومر افزایش یابد. این رابطه با معادله زیر بیان میشود:
$$M_n = (\text{Conversion}) \times \frac{[M]_0}{[I]_0} \times MW_{monomer} + MW_{initiator}$$
- اگر نمودار تجربی $M_n$ بر حسب تبدیل، یک خط راست باشد، نشاندهنده عدم وجود واکنشهای انتقال زنجیر (Chain Transfer) است.
- انحراف نمودار به سمت پایین (کاهش شیب)، نشانگر وقوع واکنشهای اختتام یا انتقال زنجیر است (مرگ زنجیرها).
- همچنین، نمودار نیمهلگاریتمی غلظت مونومر ($\ln([M]_0/[M])$) در برابر زمان باید خطی باشد که نشاندهنده ثابت بودن غلظت رادیکالهای فعال در طول واکنش (سینتیک شبه درجه اول) است.
عوامل موثر بر کاهش PDI (زیر ۱.۲) در راکتور
دستیابی به شاخص پراکندگی (Polydispersity Index – PDI) پایین، هدف نهایی در استفاده از تکنولوژی NMP است. PDI معیاری از گستردگی توزیع وزن مولکولی است و هرچه به عدد ۱ نزدیکتر باشد، پلیمر یکنواختتر است.
در سینتیک واکنش NMP، شرط لازم برای باریک شدن توزیع، «سرعت بالای تبادل» بین گونههای فعال و غیرفعال است. به زبان ریاضی، سرعت غیرفعالسازی ($R_{deact}$) باید بسیار سریعتر از سرعت رشد ($R_p$) باشد.
$$PDI = \frac{M_w}{M_n} \approx 1 + \frac{k_p [P^\bullet]}{k_{deact} [^\bullet ON]}$$
عوامل کلیدی برای کاهش PDI عبارتند از:
- غلظت مازاد نیتروکسید: وجود مقدار کمی (حدود ۵ تا ۱۰ درصد مولی) نیتروکسید آزاد اضافی در ابتدای واکنش، باعث میشود سرعت به دام افتادن رادیکالها افزایش یافته و PDI کاهش یابد.
- دمای بالا: افزایش دما معمولاً سرعت تبادل ($k_{act}/k_{deact}$) را افزایش میدهد که منجر به میانگینگیری بهتر طول زنجیرها و کاهش پهنای توزیع میشود. در سیستمهای صنعتی بهینه، رسیدن به PDI زیر ۱.۲ برای پلیاستایرن و زیر ۱.۱۵ برای آکریلاتها با این روش امکانپذیر است.
انواع مونومرهای قابل استفاده در NMP و مشکل متاکریلاتها
توسعهپذیری هر روش پلیمریزاسیون در صنعت، مستقیماً به تنوع مونومرهایی که میتواند پوشش دهد وابسته است. تکنیک پلیمریزاسیون NMP، اگرچه در ابتدا محدود به مشتقات استایرنی بود، اما با معرفی نسلهای جدید نیتروکسید، دامنه آن به طور قابل توجهی گسترش یافته است. با این حال، همچنان محدودیتهای ساختاری برای برخی گروههای عاملی وجود دارد که مهندسان شیمی باید در طراحی فرمولاسیون به آن توجه کنند.
لیست مونومرهای سازگار (استایرن، آکریلات، آکریلآمید)
موفقیت واکنش NMP به پایداری رادیکال در حال رشد و انرژی پیوند $C-O$ بستگی دارد. بر این اساس، مونومرهای NMP به دستههای زیر تقسیم میشوند:
- استایرن و مشتقات (Styrenics): این خانواده، ایدهآلترین مونومرها برای NMP هستند. رادیکالهای استایرنی پایداری رزونانسی بالایی دارند و تقریباً با تمام انواع نیتروکسیدها (از جمله TEMPO ارزانقیمت) به خوبی کنترل میشوند.
- آکریلاتها (Acrylates): بوتیل آکریلات، اتیل آکریلات و مشتقات مشابه، تنها با نیتروکسیدهای نسل دوم (مانند SG1 و TIPNO) قابل کنترل هستند. استفاده از TEMPO برای این گروه منجر به واکنشهای بسیار کند و زنجیرهای مرده میشود.
- آکریلآمیدها (Acrylamides): مونومرهایی مانند N-ایزوپروپیل آکریلآمید (NIPAM) که در ساخت پلیمرهای حساس به دما کاربرد دارند، با تنظیم دقیق شرایط و استفاده از حلالهای پروتیک، با روش NMP قابل سنتز هستند.
- دیانها (Dienes): ایزوپرن و بوتادیان نیز قابلیت پلیمریزاسیون با این روش را دارند، هرچند سرعت واکنش آنها معمولاً پایینتر از استایرن است.
چالش پلیمریزاسیون متیل متاکریلات (MMA) و راهکارهای شیمیایی
بزرگترین نقطه ضعف تکنولوژی NMP در مقایسه با ATRP و RAFT، ناتوانی ذاتی آن در پلیمریزاسیون مستقیم متاکریلاتها (به ویژه متیل متاکریلات یا MMA) است. تلاش برای پلیمریزاسیون MMA خالص با نیتروکسید، معمولاً به توقف کامل واکنش در تبدیلات پایین منجر میشود.
دلیل این شکست، واکنش جانبی مخرب «عدم تناسب» (Disproportionation) است.
در انتهای زنجیر پلیمتیلمتاکریلات، یک گروه متیل روی کربن رادیکالدار قرار دارد. به دلیل ممانعت فضایی بالا، رادیکال نیتروکسید ($^\bullet ON$) به جای اینکه با رادیکال کربن ترکیب شود (Recombination) و گونه غیرفعال را بسازد، تمایل دارد که یک اتم هیدروژن از گروه متیل همسایه (هیدروژن بتا) جدا کند.
این واکنش منجر به دو محصول پایدار و غیرفعال میشود:
- یک زنجیر پلیمری مرده با انتهای غیراشباع (پیوند دوگانه).
- یک مولکول هیدروکسیلآمین ($OH-N$) که دیگر خاصیت رادیکالی ندارد.
راهکار صنعتی:
برای غلبه بر این مشکل، روش استاندارد صنعتی استفاده از تکنیک کوپلیمریزاسیون است. افزودن مقدار کمی (حدود ۵ تا ۱۰ درصد مولی) مونومر استایرن به خوراک راکتور MMA، باعث میشود که انتهای زنجیر همواره با واحد استایرن خاتمه یابد (چون استایرن تمایل بیشتری به واکنش با نیتروکسید دارد). این تکنیک اجازه میدهد تا نیتروکسید بتواند بدون وقوع واکنش عدم تناسب، زنجیر را کنترل کند.
واکنشهای جانبی مخرب در فرآیند NMP
در تحلیل سینتیکی ایدهآل پلیمریزاسیون NMP، فرض بر این است که تنها واکنشهای موجود، تعادل برگشتپذیر بین گونههای فعال و غیرفعال و واکنش انتشار (Propagation) هستند. اما در شرایط واقعی، به ویژه در دماهای بالا و یا در حضور مونومرهای خاص، «واکنشهای جانبی» (Side Reactions) رخ میدهند که منجر به انحراف از رفتار زنده، افزایش شاخص پراکندگی (PDI) و توقف رشد زنجیر میشوند. شناخت این واکنشها برای عیبیابی فرآیند ضروری است.
مکانیزم انتقال هیدروژن بتا ($\beta$-Hydrogen Transfer) و مرگ زنجیر
اصلیترین عامل محدودکننده در کنترل پلیمریزاسیون برخی مونومرها (بهویژه متاکریلاتها)، واکنش انتقال هیدروژن بتا است.
در حالت عادی، رادیکال نیتروکسید ($^\bullet ON$) باید با رادیکال کربن ($P^\bullet$) ترکیب شود (Recombination). اما اگر ممانعت فضایی زیاد باشد، نیتروکسید ممکن است به جای جفت شدن، به عنوان یک گیرنده هیدروژن عمل کند.
در این سناریو، نیتروکسید یک اتم هیدروژن را از کربن موقعیت بتا (نسبت به مرکز رادیکالی) جدا میکند. محصولات این واکنش برگشتناپذیر عبارتند از:
- یک زنجیر پلیمری مرده با انتهای غیراشباع (پیوند دوگانه C=C).
- یک مولکول هیدروکسیلآمین ($N-OH$) که دیگر خاصیت رادیکالی ندارد.
این پدیده که منجر به «مرگ زنجیر» (Loss of Livingness) میشود، با افزایش دما و افزایش حجم گروه جانبی مونومر تشدید میگردد. معادله شیمیایی این واکنش مخرب به صورت زیر است:
$$P-CH_2-C^\bullet(R)(X) + ^\bullet ON \rightarrow P-CH=C(R)(X) + HON$$
تخریب حرارتی انتهای زنجیر در دماهای بالای ۱۳۰ درجه
اگرچه حرارت نیروی محرکه فرآیند NMP است، اما تجاوز از حد مجاز دمایی (معمولاً بالای ۱۳۰ تا ۱۴۰ درجه سانتیگراد، بسته به نوع نیتروکسید) باعث فعال شدن مسیرهای تخریب حرارتی میشود.
- تجزیه هافمن (Hofmann-like Elimination): حتی در غیاب رادیکال آزاد، گونه آلکوکسیآمین ($P-ON$) ممکن است در دماهای بسیار بالا مستقیماً دچار حذف شود و به اولفین و هیدروکسیلآمین تجزیه گردد.
- ناپایداری نیتروکسید: برخی نیتروکسیدهای نسل جدید (مانند SG1) پایداری حرارتی کمتری نسبت به TEMPO دارند و در دماهای بالا ساختار خود را از دست داده و تجزیه میشوند. این امر باعث کاهش غلظت عامل کنترلکننده و از کنترل خارج شدن واکنش میشود.
بنابراین، پنجره عملیاتی دما در راکتورهای NMP بسیار باریک است و سیستمهای کنترل دما باید دقتی در حد ±۱ درجه سانتیگراد داشته باشند تا تعادل بین سرعت واکنش و پایداری مواد حفظ شود.
تاثیر حلال و دما بر سرعت پلیمریزاسیون NMP
در طراحی فرآیند صنعتی پلیمریزاسیون NMP، انتخاب حلال (Solvent) فراتر از یک عامل رقیقکننده یا محیط انتقال حرارت است. حلالها میتوانند به طور مستقیم بر ثابت تعادل واکنش ($K$) و در نتیجه بر سرعت کلی پلیمریزاسیون ($R_p$) تأثیر بگذارند. همچنین، حرکت به سمت سیستمهای «پایه آب» (Water-based) به دلایل زیستمحیطی و مدیریت ویسکوزیته، چالشهای ترمودینامیکی جدیدی را در توزیع نیتروکسید ایجاد میکند.
نقش قطبیت حلال بر ثابت تعادل ($K$) و سرعت پلیمر شدن
مطالعات سینتیکی نشان دادهاند که سرعت پلیمریزاسیون NMP وابستگی قابل توجهی به «قطبیت حلال» دارد. این پدیده ناشی از تأثیر حلالپوشی (Solvation) بر پایداری حالت گذار و گونههای رادیکالی است.
- افزایش قطبیت: حلالهای قطبی (مانند دیمتیلفرمامید DMF یا کربنات پروپیلن) معمولاً باعث افزایش ثابت تفکیک ($k_{act}$) پیوند $C-ON$ میشوند. دلیل این امر، تثبیت بهتر ممان دوقطبی در حالت گذارِ شکستِ پیوند است. در نتیجه، غلظت لحظهای رادیکالهای فعال افزایش یافته و سرعت واکنش بیشتر میشود.
- پیوند هیدروژنی: وجود حلالهای پروتیک (مانند الکلها یا اسیدها) میتواند از طریق تشکیل پیوند هیدروژنی با اتم اکسیژنِ گروه نیتروکسید، باعث تضعیف پیوند $C-O$ و تسریع واکنش شود.
مهندسان با تنظیم پارامتر حلالیت، میتوانند بدون تغییر دما، سرعت واکنش را تا حدی دستکاری کنند. با این حال، باید مراقب بود که افزایش قطبیت منجر به افزایش واکنشهای جانبی انتقال زنجیر به حلال نشود.
اجرای NMP در سیستمهای پایه آب (امولسیون و مینیامولسیون)
اجرای NMP امولسیونی (Emulsion Polymerization) یکی از چالشبرانگیزترین حوزههای این فناوری است. مشکل اصلی در سیستمهای دوفازی (آب و روغن)، «توزیع نابرابر» (Partitioning) نیتروکسید است. اگر نیتروکسیدِ آزاد، حلالیت زیادی در آب داشته باشد، از ذرات پلیمری (فاز آلی) خارج شده و وارد فاز آبی میشود. این خروج باعث میشود که غلظت عامل کنترلکننده در محل واکنش کاهش یافته و کنترل فرآیند از دست برود.
برای حل این مشکل، صنعت به سمت تکنیک مینیامولسیون (Mini-emulsion) حرکت کرده است:
- راکتورهای نانو: در مینیامولسیون، ذرات مونومر با استفاده از نیروی برشی بالا و سورفکتانت کمکی (Co-surfactant) به قطرات بسیار ریز (۵۰ تا ۵۰۰ نانومتر) و پایدار تبدیل میشوند.
- حبس مواد: هر قطره مانند یک «نانو راکتور» مستقل عمل میکند. از آنجا که آغازگر و نیتروکسید معمولاً آبگریز (Hydrophobic) انتخاب میشوند، تمام اجزای واکنش درون قطره محبوس میمانند و مشکل انتقال جرم به فاز آبی حذف میشود.
- اثر بخشبندی (Compartmentalization): در این سیستمها، پدیدهای به نام «اثر محفظهای» رخ میدهد که میتواند به طور همزمان سرعت واکنش را بالا برده و کنترل PDI را حفظ کند؛ مزیتی که در پلیمریزاسیون تودهای (Bulk) کمتر دیده میشود.
مقایسه پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP) با ATRP و RAFT
انتخاب روش پلیمریزاسیون در مقیاس صنعتی، یک تصمیم چندوجهی بر اساس توازن میان «هزینه»، «خلوص محصول» و «تنوع مونومر» است. سه تکنیک اصلی RDRP یعنی NMP، ATRP (پلیمریزاسیون رادیکالی انتقال اتم) و RAFT (انتقال زنجیر افزایشی-قطعهقطعهشدن برگشتپذیر)، هر کدام نقاط قوت و ضعف منحصربهفردی دارند. با این حال، NMP در بازارهای خاصی که خلوص اولویت اول است، جایگاه ویژهای یافته است.
مزیت بزرگ حذف کاتالیزور فلزی (Metal-free) و کاهش هزینه تصفیه
برجستهترین مزیت رقابتی سیستم NMP نسبت به رقیب قدرتمندش ATRP، ماهیت «بدون فلز» (Metal-free) آن است.
- چالش ATRP: در فرآیند ATRP، از کمپلکسهای فلزات واسطه (مانند مس، آهن یا روتنیم) به عنوان کاتالیزور استفاده میشود. حضور حتی مقادیر ناچیز (ppm) از این فلزات در محصول نهایی، باعث تغییر رنگ، سمیت و کاهش خواص دیالکتریک میشود. بنابراین، یک مرحله پرهزینه و زمانبر «خالصسازی» (مانند ستون کروماتوگرافی یا رسوبدهی مجدد) برای حذف کاتالیزور ضروری است.
- برتری NMP: واکنش NMP صرفاً با حرارت کنترل میشود و هیچ کاتالیزور خارجی نیاز ندارد. محصول خروجی راکتور، تنها حاوی زنجیر پلیمری و گروه انتهای آلکوکسیآمین است. این ویژگی، هزینههای عملیاتی (OPEX) را به شدت کاهش داده و آن را به تنها گزینه منطقی برای کاربردهای بیومدیکال (مانند ایمپلنتها) و صنایع میکروالکترونیک (که به آلودگی فلزی حساس هستند) تبدیل میکند.
محدودیتها نسبت به RAFT در تنوع مونومرها
اگرچه NMP در خلوص برتری دارد، اما در زمینه «تنوع پذیری» (Versatility) نسبت به تکنیک RAFT محدودتر است.
- دامنه مونومر: سیستم RAFT تقریباً میتواند هر مونومری که قابلیت پلیمریزاسیون رادیکالی دارد (از جمله وینیل استات، وینیل کلراید و متاکریلاتها) را کنترل کند. در مقابل، پلیمریزاسیون NMP همانطور که در بخشهای قبل اشاره شد، در کنترل متاکریلاتها و مونومرهای با طول عمر رادیکال کوتاه، ضعف دارد.
- شرایط واکنش: عاملهای انتقال زنجیر RAFT (تیوکربونیلتیو) میتوانند در دماهای متوسط و پایین عمل کنند، در حالی که NMP نیازمند دماهای بالا (معمولاً بالای ۱۰۰ درجه) است.
- مشکلات RAFT: البته RAFT هم بینقص نیست؛ ترکیبات گوگردی مورد استفاده در آن (Dithioesters) معمولاً رنگی و دارای بوی نامطبوع هستند که حذف آنها چالشبرانگیز است، در حالی که پلیمرهای NMP معمولاً بیرنگ و بیبو هستند.
جدول مقایسه سریع:
| ویژگی | NMP | ATRP | RAFT |
| کاتالیزور فلزی | ندارد (مزیت اصلی) | دارد (نیاز به تصفیه) | ندارد |
| تنوع مونومر | متوسط (استایرن/آکریلات) | خوب | عالی (تقریباً همه) |
| دمای واکنش | بالا (High T) | متوسط | متغیر |
| وضعیت تجاری | در دسترس (SG1, TEMPO) | پرکاربرد در تحقیق | پرکاربرد در سنتز |
سنتز کوپلیمرهای قطعهای (Block Copolymers) با روش NMP
یکی از قدرتمندترین ویژگیهای پلیمریزاسیون NMP، قابلیت «شروع مجدد» زنجیرهای پلیمری است. از آنجا که انتهای زنجیرهای سنتز شده با این روش حاوی گروه فعال آلکوکسیآمین ($C-ON$) است، این زنجیرها به عنوان «ماکروآغازگر» (Macroinitiator) عمل میکنند. این ویژگی به مهندسان پلیمر اجازه میدهد تا با افزودن مونومر دوم، ساختارهای پیشرفتهای مانند کوپلیمرهای دیبلاک (AB) و تریبلاک (ABA) را طراحی کنند که در تولید الاستومرهای ترموپلاستیک و عوامل سازگارکننده کاربرد حیاتی دارند.
استفاده از ماکروآغازگرها برای تولید کوپلیمرهای دو و سه قطعهای
فرآیند سنتز کوپلیمر قطعهای در NMP طی دو مرحله متوالی انجام میشود:
- سنتز قطعه اول (A): ابتدا مونومر A پلیمریزه میشود تا به وزن مولکولی هدف برسد. محصول این مرحله، یک هموپلیمر با انتهای زنده ($P_A-ON$) است. این محصول معمولاً خالصسازی میشود تا مونومرهای واکنشنکرده حذف شوند.
- رشد قطعه دوم (B): ماکروآغازگر $P_A$ در مونومر B حل شده و دما افزایش مییابد. پیوند $C-ON$ مجدداً شکسته شده و رادیکال فعال $P_A^\bullet$ تولید میشود. این رادیکال به مونومر B حمله کرده و قطعه دوم شروع به رشد میکند.
نتیجه نهایی، زنجیری است که نیمی از آن پلیمر A و نیم دیگر پلیمر B است ($P_A-block-P_B$). اگر از آغازگرهای دوعامل (Difunctional) استفاده شود، میتوان ساختارهای سه قطعهای ABA را نیز در یک مرحله رشد دوطرفه تولید کرد.
اهمیت ترتیب اضافه کردن مونومرها در طراحی ساختار
در طراحی فرآیند تولید کوپلیمر، «ترتیب افزودن مونومرها» (Order of Addition) یک پارامتر سلیقهای نیست، بلکه توسط سینتیک تفکیک پیوند دیکته میشود.
برای داشتن یک «تبدیل (Crossover) کارآمد» از قطعه اول به دوم، سرعت شروع زنجیر دوم باید سریعتر یا هماندازه با سرعت انتشار آن باشد.
- قانون پایداری پیوند: به طور کلی، بهتر است پلیمریزاسیون را با مونومری شروع کنیم که پیوند پایدارتری با نیتروکسید تشکیل میدهد (انرژی فعالسازی بالاتر) و سپس مونومری را اضافه کنیم که پیوند سستتری دارد؟ خیر، دقیقاً برعکس.
- اگر ماکروآغازگر پیوند $C-ON$ خیلی قوی داشته باشد (مانند پلیاستایرن-TEMPO) و بخواهیم مونومری مثل آکریلات را اضافه کنیم، دمای لازم برای شکستن پیوند اولیه ممکن است برای کنترل مونومر دوم بسیار بالا باشد.
- مثال عملی: در سیستمهای مدرن مبتنی بر SG1، معمولاً توصیه میشود که ابتدا قطعه پلیآکریلات (که دمای تفکیک پایینتری دارد) سنتز شود. سپس با افزایش دما، قطعه پلیاستایرن (که نیازمند دمای بالاتر است) روی آن رشد داده شود.
- عدم رعایت این ترتیب میتواند منجر به «شروع ناقص» (Slow Initiation) شود، که در آن برخی از زنجیرهای ماکروآغازگر هرگز فعال نمیشوند و به صورت ناخالصی هموپلیمر در محصول نهایی باقی میمانند.
ساخت پلیمرهای ستارهای و شاخهدار با تکنیک NMP
یکی از جذابترین جنبههای مهندسی ماکرومولکولار با استفاده از پلیمریزاسیون NMP، توانایی عبور از ساختارهای خطی ساده و ورود به دنیای «توپولوژیهای پیچیده» است. پلیمرهای ستارهای (Star Polymers) و پلیمرهای شاخهدار (Graft Polymers) به دلیل رفتار رئولوژیکی منحصربهفرد (مانند ویسکوزیته کمتر نسبت به همتایان خطی در وزن مولکولی مشابه) و خواص مکانیکی ویژه، در صنعت مواد پیشرفته اهمیت بالایی دارند.
استراتژیهای Core-first و Arm-first در سنتز پلیمرهای پیچیده
برای سنتز پلیمر ستارهای با استفاده از سیستمهای NMP، دو استراتژی اصلی مهندسی شده است که هر کدام مزایا و معایب ترمودینامیکی خاص خود را دارند:
- رویکرد هسته-اول (Core-first):در این روش، از یک «آغازگر چند عاملی» (Multi-functional Initiator) استفاده میشود. فرض کنید یک هسته مرکزی داریم که $n$ گروه آلکوکسیآمین ($R-(ON)_n$) به آن متصل است. با اعمال حرارت، تمام این گروهها همزمان فعال شده و بازوها (Arms) به سمت بیرون رشد میکنند.
- مزیت: ساختار نهایی بسیار متقارن است و تمام بازوها وزن مولکولی یکسانی دارند.
- چالش: احتمال جفتشدن بینبازویی (Inter-arm coupling) در کانورژنهای بالا وجود دارد که منجر به تشکیل شبکه (Gelation) میشود.
- رویکرد بازو-اول (Arm-first):در این تکنیک، ابتدا بازوهای پلیمری خطی با انتهای زنده ($P-ON$) سنتز میشوند (ماکروآغازگر). سپس این بازوها در حضور یک عامل اتصالدهنده (Cross-linker) مانند دیوینیلبنزن (DVB) واکنش میدهند تا هسته مرکزی تشکیل شود.
- مزیت: امکان آنالیز دقیق وزن مولکولی بازوها قبل از تشکیل ستاره وجود دارد.
- چالش: ممکن است همه بازوها نتوانند به دلیل ممانعت فضایی به هسته متصل شوند و مقداری ناخالصی پلیمری خطی در محصول باقی بماند.
دانسیته عاملدار کردن (Functionalization) و کنترل شاخهها
برای تولید پلیمرهای شاخهدار (Graft Polymers) یا ساختارهای شانهای (Comb-like)، روش غالب در NMP تکنیک “Grafting from” است.
در این روش، ابتدا روی ستون فقرات یک پلیمر پایه (Backbone)، گروههای آغازگر آلکوکسیآمین نصب میشوند. سپس این ماکروآغازگر در محلول مونومر گرم میشود تا شاخههای فرعی از بدنه اصلی رشد کنند.
پارامتر بحرانی در این فرآیند، «دانسیته پیوندزنی» (Grafting Density) است:
- تراکم بالا: اگر فاصله گروههای آغازگر روی زنجیر اصلی خیلی کم باشد، شاخههای در حال رشد به دلیل شلوغی فضایی (Steric Crowding) مزاحم یکدیگر میشوند. این پدیده باعث میشود سرعت نفوذ مونومر به سایتهای فعال کاهش یابد و شاخهها نتوانند به طول هدف برسند (رژیم قلممو یا Brush Regime).
- کنترل با NMP: مزیت NMP در اینجا این است که با تنظیم دقیق دما و نسبت آغازگر، میتوان سرعت رشد شاخهها را کُند کرد تا از درهمرفتگی زودرس جلوگیری شود. این قابلیت در سنتز نانوذرات هیبریدی (Grafting پلیمر روی ذرات سیلیکا) کاربرد فراوانی دارد.
کاربردهای صنعتی پلیمرهای سنتز شده با NMP
گذار از آزمایشگاه به خط تولید، آزمون نهایی هر تکنولوژی پلیمریزاسیون است. کاربردهای صنعتی NMP امروزه فراتر از تولیدات آکادمیک رفته و در بازارهایی که نیازمند «معماری دقیق» و «خلوص شیمیایی» هستند، جایگاه تثبیت شدهای دارد. برخلاف پلیمریزاسیونهای متداول که برای تولید پلاستیکهای انبوه (Commodity Plastics) استفاده میشوند، NMP ابزاری برای تولید «پلیمرهای با ارزش افزوده بالا» (High-Value Polymers) است.
تولید دیسپرسکنندههای رنگدانه (Pigment Dispersants)
یکی از موفقترین بازارهای تجاری برای تکنولوژی NMP، صنعت رنگ و پوشش، به ویژه در تولید دیسپرسکنندههای رنگدانه پیشرفته است. در فرمولاسیون جوهرهای چاپ و پوششهای خودرویی، دستیابی به توزیع یکنواخت ذرات رنگدانه و جلوگیری از کلوخهای شدن (Agglomeration) آنها حیاتی است.
دیسپرسکنندههای سنتی که با روشهای رادیکالی آزاد تولید میشوند، ساختاری تصادفی (Random) دارند و کارایی پایینی ارائه میدهند. اما با استفاده از NMP، مهندسان شیمی کوپلیمرهای قطعهای آمفیفیلیک (Amphiphilic Block Copolymers) طراحی میکنند که عملکردی دوگانه دارند:
- قطعه لنگر (Anchoring Block): معمولاً شامل گروههای عاملی قطبی (مانند آمین یا اسید) است که با قدرت بالا به سطح ذره رنگدانه میچسبد.
- قطعه پایدارکننده (Stabilizing Block): این قطعه در حلال یا رزین پایه محلول است و با ایجاد ممانعت فضایی (Steric Stabilization)، مانع از نزدیک شدن ذرات رنگدانه به یکدیگر میشود.
استفاده از دیسپرسکنندههای پایه NMP منجر به کاهش ویسکوزیته خمیر رنگ، امکان افزایش بارگیری رنگدانه (Pigment Loading) و شفافیت نهایی بالاتر میشود.
کاربرد در لیتوگرافی و تولید پلیمرهای زیستسازگار
دو ویژگی ذاتی فرآیند NMP، یعنی «توزیع وزن مولکولی باریک» و «عدم استفاده از کاتالیزور فلزی»، آن را به گزینهای بیرقیب در صنایع هایتک تبدیل کرده است.
- صنایع میکروالکترونیک و لیتوگرافی:در فرآیند ساخت تراشههای نیمههادی، از پلیمرهایی به عنوان فتورزیست (Photoresist) استفاده میشود. برای دستیابی به الگوهای نانومتری دقیق، پلیمر باید دارای PDI بسیار پایین باشد. ناهمگونی در طول زنجیر پلیمری منجر به ناصافی لبهها (Line Edge Roughness) در مدارهای الکترونیکی میشود. NMP امکان تولید رزینهای اکریلاتی با ساختار دقیق و بدون آلودگیهای فلزی (که عملکرد الکتریکی چیپ را مختل میکنند) فراهم میکند.
- بیومتریال و رهایش دارو:در تولید پلیمرهای زیستسازگار (Biocompatible) برای کاربردهای پزشکی، حذف فلزات سمی (مانند مس در ATRP) یک چالش پرهزینه است. پلیمرهای سنتز شده با NMP ذاتاً فاقد فلز هستند. این پلیمرها برای ساخت حاملهای دارویی هوشمند (Drug Delivery Systems) که در پاسخ به دما یا pH بدن دارو آزاد میکنند، و همچنین در تولید ایمپلنتهای پلیمری تجزیهپذیر استفاده میشوند. خلوص بالای محصول نهایی، تاییدیههای سازمانهای بهداشتی (مانند FDA) را تسهیل میکند.
روشهای آنالیز پلیمر NMP؛ طیفسنجی ESR و کروماتوگرافی GPC
تأیید صحت انجام پلیمریزاسیون NMP و اطمینان از «زنده بودن» (Livingness) زنجیرهای پلیمری، نیازمند ابزارهای دقیق آزمایشگاهی است. برخلاف پلیمریزاسیونهای متداول که تنها اندازهگیری ویسکوزیته یا وزن نهایی کفایت میکند، در NMP باید دینامیک حضور رادیکالها و تکامل توزیع جرم مولکولی به دقت پایش شود. دو تکنیک اصلی برای این منظور، طیفسنجی رزونانس پارامغناطیس الکترون (ESR) و کروماتوگرافی ژلتراوا (GPC) هستند.
استفاده از ESR برای ردیابی غلظت رادیکالهای نیتروکسید
تکنیک طیفسنجی ESR (که گاهی EPR نامیده میشود)، تنها روش مستقیم برای شناسایی و اندازهگیری غلظت گونههای دارای الکترون جفتنشده (رادیکالها) در محیط واکنش است.
از آنجا که عامل کنترلکننده در این فرآیند یک رادیکال پایدار (نیتروکسید) است، ESR ابزار قدرتمندی برای مطالعه سینتیک آن محسوب میشود.
- تشخیص رادیکال آزاد: دستگاه ESR میتواند غلظت رادیکالهای نیتروکسید آزاد ($^\bullet ON$) را حتی در مقادیر بسیار ناچیز (در حد $10^{-7}$ مولار) ردیابی کند. الگوی طیفی (Hyperfine Splitting) حاصل، اطلاعات دقیقی درباره ساختار شیمیایی نیتروکسید و محیط اطراف آن ارائه میدهد.
- تأیید اثر رادیکال پایدار: محققین با استفاده از ESR، افزایش تدریجی غلظت نیتروکسید آزاد در طول زمان را مشاهده میکنند. طبق «قانون فیشر»، این افزایش غلظت دقیقاً منطبق بر نمودار کاهش سرعت پلیمریزاسیون است و اثبات میکند که مکانیزم خودتنظیمی PRE در حال اجراست.
تحلیل دقیق توزیع وزن مولکولی با GPC
برای مهندسی که محصول نهایی را بررسی میکند، دادههای حاصل از آنالیز GPC (یا SEC) حکم شناسنامه محصول را دارد. این آزمون با جداسازی زنجیرهای پلیمری بر اساس حجم هیدرودینامیکی، نمودار توزیع وزن مولکولی را رسم میکند.
تفسیر نمودارهای GPC در سیستم NMP حاوی نکات فنی زیر است:
- محاسبه PDI: پارامتر کلیدی، شاخص پراکندگی ($PDI = M_w/M_n$) است. مقادیر زیر ۱.۲ برای استایرن و زیر ۱.۳ برای آکریلاتها، نشاندهنده کنترل عالی بر فرآیند است.
- تقارن پیک: نمودار باید تکمُدی (Unimodal) و متقارن باشد. وجود «شانه» (Shoulder) در سمت وزنهای مولکولی بالا، نشاندهنده وقوع واکنش اختتام دومولکولی (جفتشدن زنجیرها) است.
- دنباله (Tailing): وجود دنباله در سمت وزنهای مولکولی پایین، معمولاً ناشی از شروع کُند (Slow Initiation) یا واکنشهای انتقال زنجیر است.
- شیفت کامل: در سنتز کوپلیمرهای قطعهای، تزریق نمونه به GPC باید نشان دهد که پیک اولیه ماکروآغازگر به طور کامل به سمت وزنهای مولکولی بالاتر جابجا شده است؛ عدم جابجایی کامل به معنای وجود زنجیرهای مرده در ماکروآغازگر است.
آینده تکنولوژی NMP؛ روشهای نوری و دمای محیط
با وجود بلوغ نسبی فرآیند NMP در صنعت، تحقیقات برای رفع پاشنه آشیل اصلی آن، یعنی «دمای بالای واکنش» (High Temperature)، همچنان ادامه دارد. نیاز به انرژی حرارتی بالا (بالای ۱۲۰ درجه) نه تنها هزینه انرژی را افزایش میدهد، بلکه استفاده از NMP را برای مونومرهای حساس به دما و زیستتخریبپذیر محدود میکند. نسل آینده این فناوری بر پایه روشهای «غیرحرارتی» استوار است.
جایگزینی حرارت با نور UV برای فعالسازی آلکوکسی آمین
رویکرد Photo-NMP (NMP نوری) یکی از جذابترین مرزهای دانش در شیمی پلیمر است. در این روش، انرژی لازم برای شکستن همولیتیک پیوند $C-ON$، نه از طریق ارتعاشات حرارتی، بلکه از طریق جذب فوتونهای نور (معمولاً محدوده UV یا نور مرئی آبی) تأمین میشود.
مزیتهای مهندسی این روش عبارتند از:
- انجام واکنش در دمای اتاق: نور UV میتواند پیوند حساس به نور در آلکوکسیآمینهای اصلاحشده را بشکند، بدون اینکه نیاز به گرم کردن کل راکتور باشد.
- کنترل مکانی-زمانی (Spatiotemporal Control): واکنش پلیمریزاسیون تنها زمانی و مکانی رخ میدهد که نور تابیده شود. به محض خاموش کردن منبع نور، تولید رادیکال متوقف شده و واکنش فریز میشود. این ویژگی قابلیت بینظیری برای کاربردهای لیتوگرافی، چاپ سهبعدی و الگوهی سطح فراهم میکند.
توسعه سیستمهای کاتالیزوری برای انجام واکنش در دمای اتاق
علاوه بر نور، شیمیدانان به دنبال کاتالیزورهای شیمیایی هستند که بتوانند انرژی فعالسازی تفکیک آلکوکسیآمین را کاهش دهند. تحقیقات اخیر نشان داده است که استفاده از مقادیر اندکی از اسیدهای لوئیس یا عوامل اکسیدکننده/کاهنده میتواند ثابت سرعت تفکیک ($k_d$) را به شدت افزایش دهد.
این رویکرد که به “Room Temperature NMP” معروف است، هنوز در مرحله تحقیق و توسعه (R&D) قرار دارد، اما پتانسیل آن را دارد که NMP را به رقیبی جدی برای ATRP در سنتز پلیمرهای زیستی حساس تبدیل کند، بدون اینکه خلوص محصول نهایی با فلزات سنگین به خطر بیفتد.
نتیجه گیری
در این مقاله جامع، پلیمریزاسیون رادیکالی کنترل شده با نیتروکسید (NMP) را به عنوان یک تکنولوژی بالغ و بدون فلز (Metal-free) در صنعت پلیمر مورد تحلیل قرار دادیم. انتخاب NMP برای یک واحد تولیدی، انتخابی بر مبنای توازن میان «هزینه مواد اولیه» و «هزینه فرآیند پاییندستی» است.
اگرچه قیمت آغازگرهای آلکوکسیآمین (مانند BlocBuilder) نسبت به کاتالیزورهای مس در روش ATRP بالاتر است، اما حذف کامل مراحل تصفیه و شستشو در NMP، این اختلاف هزینه را در مقیاس صنعتی جبران میکند. برای تولیدکنندگانی که هدفشان بازارهای حساس مانند پزشکی، آرایشی-بهداشتی و الکترونیک است، NMP به دلیل خلوص ذاتی محصول و سادگی فرآیند (تنها یک مرحله حرارتی)، منطقیترین گزینه مهندسی محسوب میشود. در مقابل، برای تولیدکنندگانی که نیاز به پلیمریزاسیون طیف وسیعی از مونومرهای نامتعارف (غیر استایرنی/آکریلاتی) دارند، روشهای RAFT یا ATRP ممکن است ارجحیت داشته باشند.